Número:
- Vol. 3
- Num. 18
- Noviembre - Diciembre
Avicultura.mx
Autores:
 Jesús
Jesús Sánchez Hernández
Nacionalidad: Mexicana
Grado académico: Ing. en Biotecnología
 Víctor Manuel
Víctor Manuel Hernández Pimentel
 D. V.
D. V. Melo Sabogal
 E. N.
E. N. García Sánchez
ISSN-e:
2992-7293
Efecto de agua electrolizada neutra sobre la desinfección y propiedades físicoquímicas del huevo de gallina (Gallus domesticus)
RESUMEN
El huevo de gallina es un alimento de alto valor proteico en la alimentación de los humanos. México ocupa el primer puesto como consumidor de huevo y el quinto lugar como productor con 3 millones 26 mil toneladas. En nuestro país, no está permitido el lavado de huevo para su comercialización mientras que, en otros países como Estados Unidos, se emplea el lavado de huevo con agua y algunos agentes químicos. El agua electrolizada neutra (AEN) es un agente antimicrobiano de amplio espectro, que se ha venido utilizando en los últimos años en la industria alimentaria, debido a ciertas ventajas que presenta sobre otros agentes como bajo costo de producción, baja o nula toxicidad, producción in situ, y no genera residuos tóxicos. El objetivo de este proyecto es determinar el efecto del AEN sobre la desinfección y propiedades fisicoquímicas del huevo de gallina (Gallus domesticus). Se realizó un reto microbiano contra S. Typhimurium inoculada en la superficie de huevo y se evaluó su efecto sobre las propiedades fisicoquímicas del cascarón como el color (Cielab), grosor (μm) y superficie mediante SEM. El AEN a 50 ppm presenta una reducción antimicrobiana de (2.3 log UFC/mL) similar al NaClO (50 ppm) y al ácido peracético (150 ppm) sobre Salmonella Typhimurium. El AEN no presenta cambios significativos en el cambio de color (ΔE) con respecto a los demás tratamientos, mientras que el AEN fue quien menos redujo el grosor del cascarón del huevo de gallina. El tratamiento con AEN presenta grietas de menor tamaño en comparación con el tratamiento de NaClO y no presenta poros, lo que indica que tiene un menor efecto sobre la superficie del cascarón de huevo con una superficie más parecida al grupo control con agua.
Palabras clave: huevo, desinfección, agua electrolizada neutra, salmonella, propiedades fisicoquímicas
INTRODUCCIÓN
La producción de huevo de gallina ha sido constantemente intervenida por el humano para aumentar la cantidad y la calidad del producto. En la industria avícola, existen diversas razas de aves que son utilizadas para producción de huevo como Leghorn, Lohmann, Hy line, de Kalb, Shaver, entre otras. Una gallina criolla puede poner en promedio de 125 huevos por año, mientras que una gallina de postura puede llegar a poner 300 huevos al año (Molnár et al., 2017). La Unión Nacional de Avicultores (UNA, 2020) informó que, México ocupa el 5° lugar de producción de huevo a nivel mundial detrás de China, India, Estados Unidos y Brasil mientras que, como consumidor ocupa el 1er lugar 24.21 kg (per capita anual). Los principales estados productores en México son Jalisco (53.9%), Puebla (15.9 %), Sonora (5.1 %) y Nuevo León (2.9 %).
El huevo está conformado por tres principales partes: la yema (27 - 32%), la clara o albúmina (56 - 61%) y cascarón (8 - 11%). El cascarón está conformado por la cutícula, el empalizado, el mamilar y las membranas. La cutícula es la capa más externa del huevo, brinda protección contra microrganismos además previene la pérdida excesiva de agua a través de los poros y está compuesta por 87% de proteínas, 4.4% carbohidratos y 3.5% de lípidos. El empalizado es una capa pegada a la cutícula en la parte interna, está compuesta principalmente por CaCO3. La capa mamilar, donde comienza la mineralización, se integra por pequeñas masas de material orgánico formadas por un complejo de proteínas-mucopolisacáridos que se unen a la superficie externa de la membrana y es donde se depositan los cristales de calcita formando conos (García, 2015). Finalmente, la capa de membranas que está compuesta por fibras proteicas rodeadas por mucopolisacáridos y es la capa más interna del cascarón haciendo la frontera entre el contenido líquido, aunque se permite el intercambio gaseoso (Cascarín, et al., 2023).
Los principales factores que determinan la calidad del cascarón son el grosor y la resistencia al quiebre, factores que derivan en una gran pérdida económica para la industria avícola en caso de una mala calidad (Cascarín, et al., 2023). La calidad del huevo también está relacionada con su carga microbiana, así como por otras propiedades físicas del cascarón como la textura y color. Durante un almacenamiento prolongado se degrada el albumen y se modifica la interacción entre ovomucina y lisozima, lo que aumenta el intercambio gaseoso entre el interior del huevo y el medio ambiente. La temperatura de conservación del huevo debe estar entre 18 y 22°C, ya que una temperatura mayor conlleva a una pérdida de CO2, lo que genera un aumento de pH en la clara y con ello pérdidas ya que, se favorece la contaminación interna del huevo. Una humedad relativa baja acelera la pérdida de agua del huevo mientras que una humedad relativa elevada) favorece el desarrollo de hongos y bacterias en la superficie (Bedoya, 2020).
Muchos alimentos, en específico los de origen animal, han sido identificados como vehículos de transmisión de ciertos microorganismos patógenos, puntualmente se reconoce a las aves de corral son un reservorio de la bacteria Salmonella. Éste patógeno reside naturalmente en el tracto intestinal y también se expulsa en las heces de animales y humanos infectados. El contenido del huevo puede contaminarse por 2 vías: transovárica (transmisión vertical) donde el patógeno se introduce desde los tejidos reproductivos infectados antes de la formación de la cáscara y los serotipos asociados con esta vía de contaminación son S. Enteritidis, S. Typhimurium y S. Heidelberg. La transmisión transcáscara u horizontal, suele asociarse con la contaminación fecal de la cáscara del huevo por el animal que lo expulsa o por otros vectores ambientales, como agricultores, mascotas y roedores. Por otro lado, es posible que el contenido del huevo se contamine por una migración a través de la cáscara y las membranas del huevo si las cáscaras de huevo están húmedas, así como por el almacenamiento a temperatura ambiente y el daño en estructura de la cáscara (Kirunda & McKee, 2000).
Los desinfectantes son sustancias que destruyen microorganismos y son aplicados en superficies inertes (principalmente en industria alimentaria) ya que se utilizan concentraciones que pueden intoxicar o ser irritantes de ser aplicadas en organismos vivos o alimentos (Gonzales, 2003). En México, la legislación no permite el lavado de huevo con desinfectantes durante su procesamiento para ser comercializado únicamente se permite el lavado de la canal con agua fría (NOM-159-SSA1-2016). Diversos agentes son empleados de manera común en la industria alimentaria y que están permitidos en el sector avícola en otros países como Estados Unidos. El hipoclorito de sodio (NaClO) es un desinfectante comercial eficiente de un amplio espectro bactericida y bajo costo, sin embargo, si es utilizado en concentraciones mayores a 100 ppm resulta ser tóxico ya que forma compuestos los trihalometanos (THM) con potencial carcinogénico por la oxidación de materia orgánica (EPA, 1999). El ácido peracético (AP) es también ampliamente utilizado por su gran poder desinfectante y no presentan efectos carcinogénicos ni mutagénicos ni genera residuos tóxicos (Aguayo et al., 2017). La norma española EN-13697 permite utilizar el ácido peracético en concentraciones inferiores a 150 ppm y su aplicación puede ser mediante aspersión o inmersión. Sin embargo, el AP es una sustancia química sumamente corrosiva y una inapropiada manipulación puede producir graves irritaciones y quemaduras en la piel y ojos por lo que se requiere utilizar equipo de protección y destreza del personal durante su manipulación (Moreno, 2014). El agua electrolizada neutra (AEN) se produce mediante electrólisis con solución salina de NaCl 1 a 3% sometida a una corre eléctrica (9 - 120 V y 0.7 -20 A). Durante el proceso electrolítico se forman iones de carga negativa que migran al ánodo donde pierden electrones y se forma el ácido hipocloroso (HOCl), ion hipoclorito (-OCl), ácido clorhídrico (HCl), oxígeno (O2) y cloro gaseoso (Cl2), mientras que, los iones de carga negativa migran al cátodo donde se ganan electrones y se forma hidróxido de sodio (NaOH) e hidrógeno (H2)g. Al no emplear una membrana diafragmática que separe los iones formados, se obtiene AEN con un pH de 7 a 8 con ORP cercano a 990 mV lo que le atribuye un amplio espectro y alto poder oxidante (Tabernero de Paz et al., 2013; Rahman et al., 2016). El AEN es permitida en la industria avícola en Estados Unidos, si no excede la concentración máxima que es de 50 ppm en un proceso de inmersión (FSIS, 2012).
METODOLOGÍA – MATERIALES Y MÉTODO
Material biológico
La cepa utilizada en esta investigación fue S. Typhimurium ATCC 14028 conservada en ultracongelación a -52°C. Las muestras de huevo empleadas para el análisis microbiológico fueron obtenidas en un supermercado local, mientras que las muestras de huevo empleadas para los análisis fisicoquímicos se obtuvieron con un pequeño productor, con el fin de garantizar que no hubieran tenido tratamiento alguno previo.
Determinación de la actividad antimicrobiana de AEN sobre S. Typhimurium
Se procedió según lo reportado por Hernández-Pimentel et al, (2020). Preparación del inóculo: La cepa se descongeló y realizó una primera activación donde se colocó una chaquira de vidrio con el microorganismo un matraz con 50 mL con medio de caldo Soya Tripticaseína (CST) se incubó durante 24 h a 37°C. Se realizó una segunda activación con 0.1 mL del primer matraz y se inoculó un segundo matraz y se incubó a las mismas condiciones. Se colocaron 50 mL de la segunda activación y se centrifugaron a 4000 rpm durante 10 min. Se retiró el sobrenadante y se agregaron 10 mL de solución salina estéril (SS) a 0.9 % (p/v) y se resuspendió la pastilla. Se repitió el lavado dos veces a las mismas condiciones para obtener la una solución stock del inóculo. Se ajustó la población del microorganismo a una población de 6 log UFC/mL.
Se emplearon 45 huevos para este experimento con una unidad experimental de un huevo por cada tratamiento. Se empleó un tratamiento de AEN a 50 ppm, dos controles positivos de hipoclorito de sodio (NaClO) a 50 ppm, y ácido peracético (AP) a 150 ppm y un control negativo con agua para ver el efecto de arrastre. Se desinfectó con etanol al 70% /v/v) y se inoculó la superficie del cascarón de cada huevo con 1 mL del inóculo y se dejó un tiempo de adhesión de 10 min en campana de flujo laminar. Cada huevo inoculado, se sumergió en 90 mL de cada tratamiento durante 10 min y posteriormente, se sumergió y frotó durante 2 min en 90 mL de agua peptonada estéril para la recuperar las bacterias tratadas sobrevivientes. Se realizaron diluciones decimales seriadas e inocularon cajas Petri con agar soya tripticaseína (AST) mediante el método Miles-Misra y se incubaron a 37 °C durante 24 h. Se realizaron tres réplicas experimentales.
Determinación del efecto de AEN en las propiedades fisicas
Se emplearon un total de 36 piezas tanto para la determinación de color como para la determinación de grosor. Se empleó un tratamiento de AEN a 50 ppm, dos controles positivos con NaClO (50 ppm), y AP (150 ppm) y un control negativo con agua. Cada huevo, como unidad experimental, se sumergió en 100 mL de cada tratamiento durante 10 min y se dejaron secar.
Determinación de color: se procedió según lo reportado por (Li, et al., 2020) con un colorímetro portátil modelo CS-10 (CHN Spec, Cantón, China.) mediante sistema de coordenadas CIELab*. Se tomaron 3 repeticiones de lecturas de color en tres diferentes zonas (superior, ecuatorial e inferior). Se realizaron tres réplicas experimentales.
Determinación de grosor: se procedió según lo reportado por (Guzmán-Guzmán et al., 2018). El grosor del cascarón de huevo fue medido mediante un micrómetro digital modelo FTVOGUE (marca Astyer-X, Zhejiang, China). Posterior a los tratamientos, se realizó un orificio de 1 cm de diámetro en el cascarón para vaciar su contenido y se dejó secar a temperatura ambiente durante 24 h. Las lecturas fueron tomadas en las mismas zonas donde se midió el color.
Visualización de la superficie del cascarón mediante SEM: Se cortó una muestra de 1 cm2 y se observó al microscopio (Carl Zeiss, EVO 50, Alemania). Las condiciones para la microscopia electrónica de barrido fueron: rango de aumento 150x, 100x y 2500x, voltaje de aceleración 10kV, alto vacío 4×10−4mBa y previo recubrimiento por ionización catódica (Denton Vaccum, Desk ll, NJ, EUA) con oro a cada muestra (Medina-Gudiño, et al., 2020).
RESULTADOS Y DISCUSIÓN
Para el reto microbiano, el grupo control con agua, permitió visualizar el efecto de arrastre por el lavado de huevo en el que se recuperó una población de 4.1 log UFC/mL. El tratamiento con AEN (50 ppm) no tuvo diferencia significativa con los controles positivos (NaClO 50 ppm ni AP 150 ppm) con una reducción total del inóculo poco mayor a 2 log UFC/mL (Tabla 1). El AEN actividad antimicrobiana similar al AP con una concentración tres veces inferior lo que pudiera implicar una ventaja en gasto, además de que no resulta tan tóxico e irritante como el AP en su manipulación. Por otro lado, el AEN tuvo mismo efecto antimicrobiano que el NaClO, lo cual indica que pudiera representar una alternativa en la industria avícola ya que el NaClO está prohibido su uso en muchos países en contacto directo con alimentos por la generación de residuos tóxicos (Hernández-Pimentel, et al., 2020).

Medina-Gudiño et al., (2020) observaron una reducción de S. entérica de 1.45 log UFC/pieza al emplear 60 ppm de AEN. De manera similar, Rivera et al., (2019) observaron una reducción de L. monocytogenes de 2.18 log UFC/pieza. Otros autores han demostrado el efecto bactericida de AEN 50 ppm sobre Salmonella en diversos alimentos como lechuga, zanahoria, escarola, jícama, tomate, aguacate y queso Oaxaca, obteniendo como resultado la reducción de la población de hasta 3 log UFC/mL (Abadias et al., 2008; Cadena, 2014).
Determinación del efecto del AEN en el grosor del cascarón de huevo
Al analizar el grosor del cascarón se observó diferencia significativa entre los tratamientos de AP con a AEN y control con agua teniendo el AP los valores más bajos en grosor del cascarón. Los tratamientos con AEN y agua no presentan una diferencia estadísticamente significativa. Se observó que el cascarón no presenta uniformidad en su grosor ya que en la zona ecuatorial es más delgado y en el inferior es más grueso.
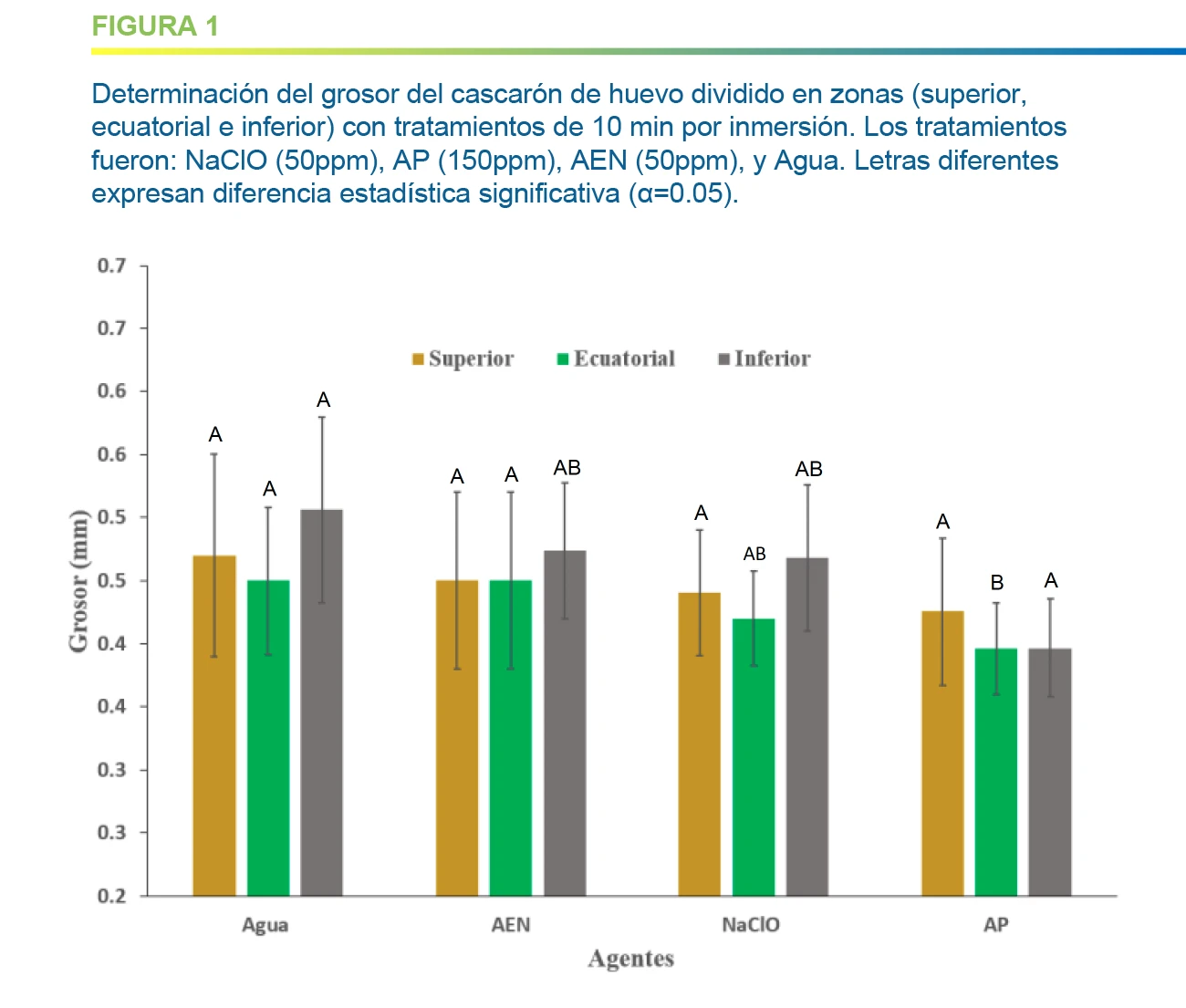
Determinación del cambio de color del cascarón de huevo de gallina después del tratamiento de desinfección.
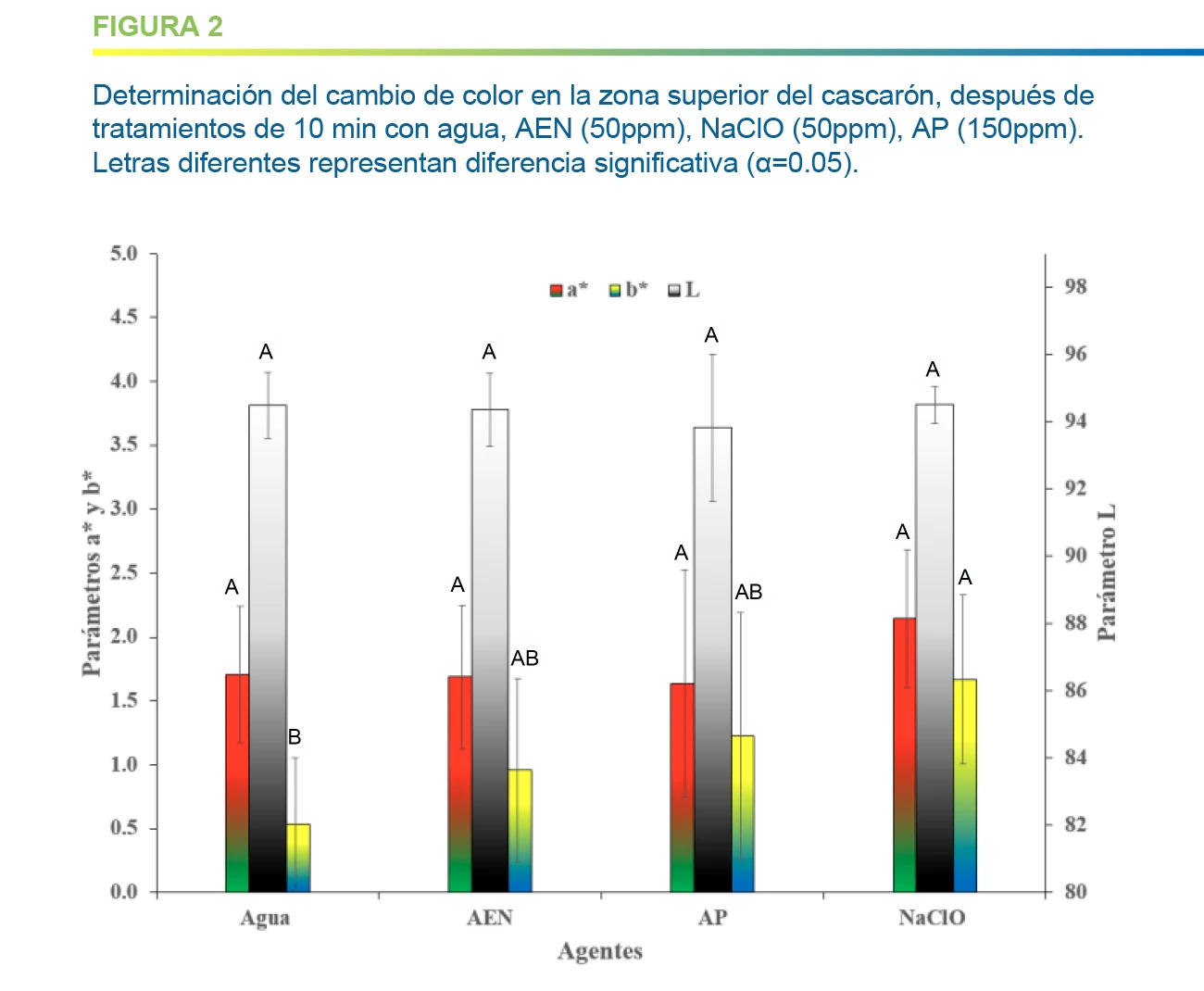
En cuanto a las mediciones de color en zona superior, y para los parámetros de color L* (luminosidad)y a* (tonalidad roja) no se aprecia diferencia estadísticamente significativa. El AEN a 50 ppm no presenta diferencia significativa con ninguno de los tratamientos en el cambio de coloración (ΔE). El NaClO (50ppm) presenta diferencia significativa con relación al control con agua en el parámetro b* que está relacionado con la escala en coloración amarilla, lo que implica que los huevos tratados con este agente presentan una coloración ligeramente más amarillenta.
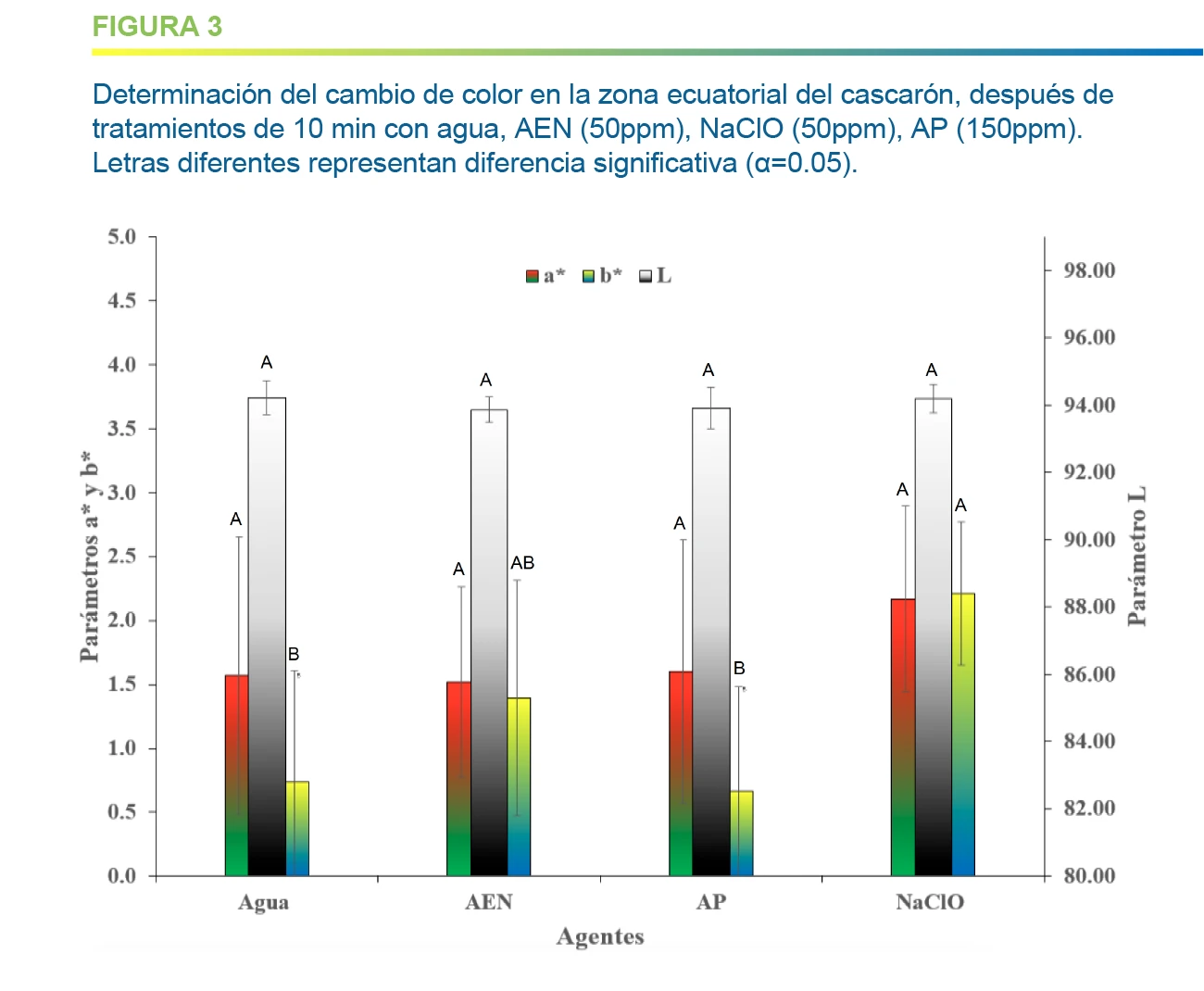
En cuanto a las mediciones de color en zona ecuatorial, y para los parámetros de color L* (luminosidad)y a* (tonalidad roja) no se aprecia diferencia estadísticamente significativa. El AP presenta diferencia significativa estadística con respecto a NaClO. Es interesante que, el AEN a 50 ppm no presenta diferencia significativa estadística con los demás controles, lo que significa que el AEN no produjo un cambio de color que sea significativo. El NaClO fue el agente que obtuvo cambios orientados a valores más positivos según el sistema de coordenadas CIEL*a*b*, implicando una mayor coloración.
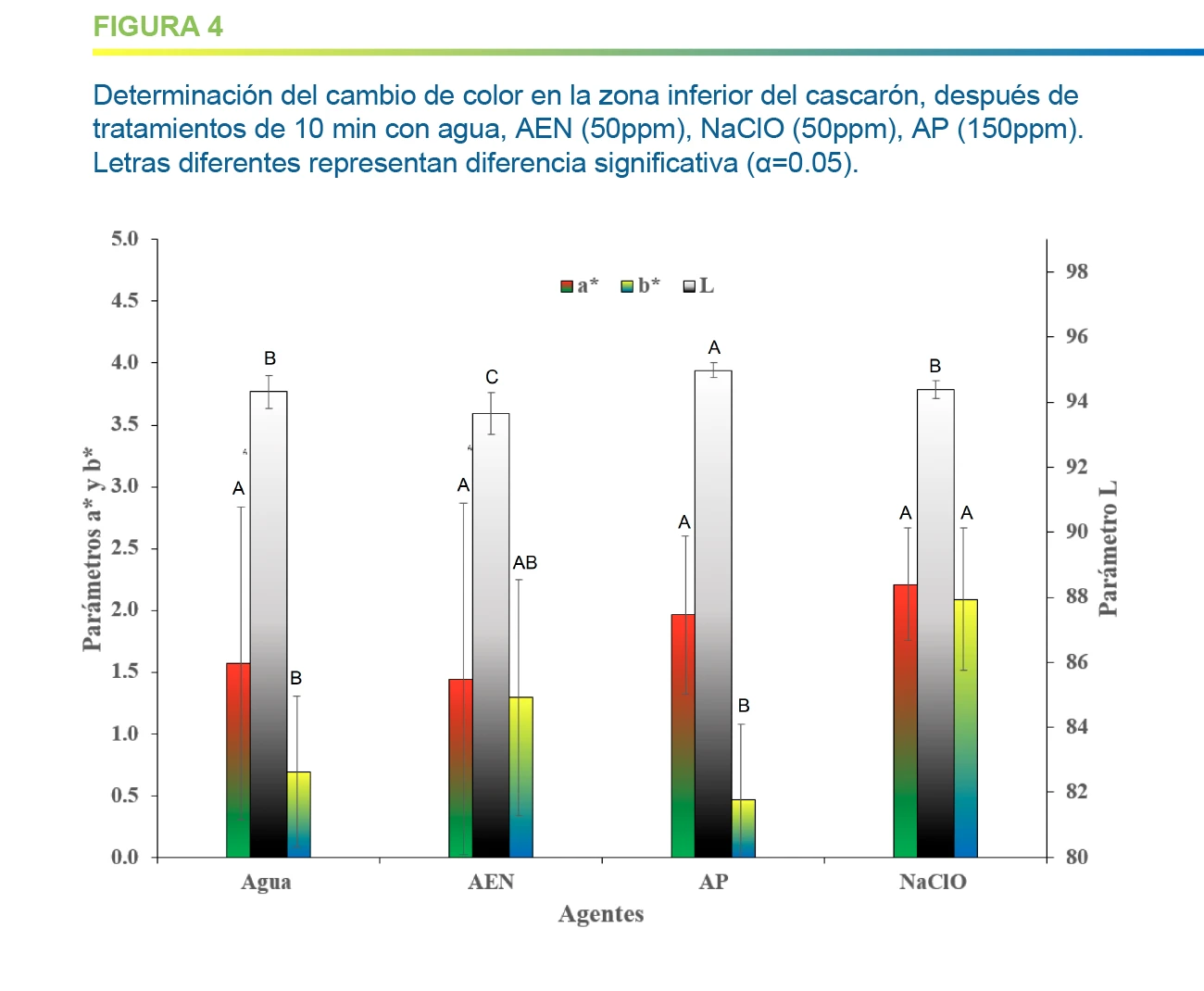
Para la zona inferior, no se observó diferencia significativa en el parámetro a*, sin embargo, para el parámetro L* solamente los tratamientos NaClO y control de agua no mostraron diferencia significativa. Hernández-Pimentel et al. (2020), observó que la carne de pollo presentó un efecto al ser tratada con NaClO así como con AP (principalmente donde había golpes en las canales) mientras que, con AEN observó que el cambio de color fue similar al grupo control con agua. Los autores analizan que dicho efecto es posible que sea debido a que el AEN está reportado que sufre una inactivación muy rápida en presencia de materia orgánica, lo que limita su efecto continuo a diferencia de otros agentes que se inactivan de un modo más lento y su efecto es mayor.
Microscopía de barrido en cascarón de huevo de gallina.
En la Figura (5) se puede observar que con AP hay una abundante cantidad de poros, lo que puede indicar que la capa de la cutícula conformada por proteínas, carbohidratos y lípidos este viéndose afectada en concordancia con Wellman, et al. (2014). Del mismo modo, con agua, AEN y NaClO se pueden observar una mayor concentración de formaciones vesiculares, así como la presencia de grietas expuestas, sin embargo, es importante mencionar que con NaClO las gritas eran más abundantes y de mayor tamaño y profundidad.

En este sentido, el uso de AEN podría implicar una ventaja ya que por un lado, tiene poder desinfectante similar al AP y al NaClO, pero estos dos agentes podrían facilitar el ingreso de agentes o sustancias contaminantes al interior del huevo y permitir asimismo un aumento en la transferencia de oxígeno e incluso la pérdida excesiva de agua (Bedoya, 2020). Medina-Gudiño et al. (2020) observaron que la cutícula del huevo de gallina muestra fisuras que relaciona con el aspecto del barro seco producido por la deshidratación de los grupos sulfhidrilo (SH) de las proteínas siendo una barrera muy importante para la calidad del huevo.
De manera general, el ácido peracético es considerado un ácido fuerte y por lo tanto es corrosivo y puede irritar piel, mucosas, ojos y tracto respiratorio. El AEN es una sustancia que se considera segura a pesar de tener mayoritariamente un ácido en su composición, no es corrosivo, tampoco tóxico y al entrar en contacto con materia orgánica se inactiva fácilmente.
CONCLUSIONES Y PERSPECTIVAS
La capacidad desinfectante del AEN a 50 ppm presenta una reducción de la población de Salmonella, similar a la de NaClO (50 ppm) y al AP (150 ppm) resaltando que este último fue utilizado en una concentración 3 veces mayor. En cuanto al grosor del cascarón, el AEN no presenta diferencia significativa entre el control (agua) y el NaClO (50 ppm), a diferencia del AP (150ppm) el cual redujo significativamente el grosor del cascarón. El AEN no presenta cambios significativos en el cambio de color (ΔE) con respecto a los demás tratamientos, además de ser quien presenta ser el agente de menor actividad corrosiva sobre la estructura superficial del cascarón de gallina.
REFERENCIAS
Abadias, M., Usall, J., Oliveira, M., Alegre, I., & Viñas, I. (2008). Efficacy of neutral electrolyzed water (NEW) for reducing microbial contamination on minimally-processed vegetables. International Journal of Food Microbiology, 123(1-2), 151-158. https://doi.org/10.1016/j.ijfoodmicro.2007.12.008.
Aguayo, E., Gómez, P., Artés-Hernández, F., & Artés, F. (2017). Tratamientos químicos desinfectantes de hortalizas de IV gama: Ozono, agua electrolizada y ácido peracético. Agrociencia, 21(1), 7-14. https://doi.org/10.31285/agro.21.1.2.
Bedoya, S. (2020). Usos potenciales de la cáscara de huevo de gallina (Gallus gallus domesticus): Una revisión sistemática. https://doi. org/10.24188/recia.v12.n2.2020.776.
Bustamante, M. (2014). Avances en los sistemas de limpieza y desinfeccion aplicados en la industria alimentaria. Universidad Pontificia Bolivariana, 66.
Cadena, Mo., E. E. (2014). Estudio dela aplicación de agua electrolizada neutra en la desinfección de frutas y hortalizas frescas. Tesis de Maestría en Ciencias de los Alimentos. Universidad Autónoma de Queretaro.
Casarín A., Villar G. & Olvera-García M. (2023). Factores que afectan la calidad de la cáscara del huevo para consumo humano. Obtenido de www. https://www.avicultura.mx/destacado/factores-que-afectan-la-calidad-de-la-cascara-del-huevo-para-consumo-humano.
Environmental Protection Agency (EPA). (1999). Alternative Disinfectants and Oxidants Guidance Manual. Extraído de https://eec.ky.gov/Environmental-Protection/Water/Drinking/DWProfessionals/ComplianceDocuments/Alternative%20Disinfection%20and%20Oxidants%20Guidance%20Manual.pdf.
Food Safety and Inspection Service (FSIS). (2012). Directive USDA/FSIS, Washington, DC: Last review December 21th 2012. Safe and suitable ingredients used in the production of meat, poultry and egg products.
García, Campos, T. (2015). Extracción y aplicaciones alimentarias de membranas de cáscara de huevo. Tesis de Maestría en Biotecnología Alimentaria en la Universidad de Oviedo.
Gonzáles, L. (2003). Antisepticos y desinfectantes. Educacion Sanitaria, 22, 64-70.
Guzmán-Guzmán, M., Zuñiga, H., Moreno S, J. A., & GRANADOS M, J. E. (2018). Estudio físico-químicos de los huevos de Iguana iguana Linnaeus, 1758. Revista Colombiana de Ciencia Animal - RECIA, 10(2), 124-130. https://doi.org/10.24188/recia.v10.n2.2018.648
Hernández-Pimentel, V. M., Regalado-González, C., Nava-Morales, G. M., Meas-Vong, Y., Castañeda-Serrano, M. P., and García-Almendárez, B. E. (2020). Effect of neutral electrolyzed water as antimicrobial intervention treatment of chicken meat and on trihalomethanes formation. J. Appl. Poult. Res. 29, 622–635. doi: 10.1016/j.japr.2020.04.001
Kirunda, D. F. K., & McKee, S. R. (2000). Relating Quality Characteristics of Aged Eggs and Fresh Eggs to Vitelline Membrane Strength as Determined by a Texture Analyzer. Poultry Science, 79(8), 1189–1193. doi:10.1093/ps/79.8.1189.
Landa-Solis, C., González-Espinosa, D., Guzmán-Soriano, B., Snyder, M., Reyes-Terán, G., Torres, K., & Gutierrez, A. A. (2005). MicrocynTM: A novel super-oxidized water with neutral pH and disinfectant activity. Journal of Hospital Infection, 61(4), 291-299. https://doi.org/10.1016/j.jhin.2005.04.021
Li, Q., Ren, J., Wang, K., Zheng, J., Xu, G., Ge, C., … Sun, C. (2020). The effect of breed and age on the gloss of chicken eggshells. Poultry Science, 99(5), 2494–2499. doi:10.1016/j.psj.2020.01.010.
Medina-Gudiño, J., Rivera-Garcia, A., Santos-Ferro, L., Ramirez-Orejel, J. C., Agredano-Moreno, L. T., Jimenez-Garcia, L. F., … Cano-Buendia, J. A. (2020). Analysis of Neutral Electrolyzed Water anti-bacterial activity on contaminated eggshells with Salmonella enterica or Escherichia coli. International Journal of Food Microbiology, 320, 108538. doi:10.1016/j.ijfoodmicro.2020.10853.
Molnár, A., Zoons, J., Buyse, J. & Delezie, E. (2017). Extender el ciclo de puesta de las gallinas ponedoras: ¿se puede mantener la calidad del huevo? Presentado en el 17º simposio europeo sobre la calidad de huevos y productos de huevo (p. 30).
Moreno, B. C. (2014). Riesgos a la salud humana derivados de la exposición por manejo y almacenamiento de sustancias químicas en los establecimientos comerciales e industriales de Bogotá durante el 2013. Recuperado de: http://hdl.handle.net/10654/13347.
Norma Oficial Mexicana NOM-159-SSA1-2016, Productos y servicios. Huevo y sus productos. Disposiciones y especificaciones sanitarias. Métodos de prueba.
Rahman, S., Khan, I., & Oh, D. H. (2016). Electrolyzed Water as a Novel Sanitizer in the Food Industry: Current Trends and Future Perspectives. Comprehensive Reviews in Food Science and Food Safety, 15(3), 471-490. https://doi.org/10.1111/1541-4337.12200.
Tabernero de Paz, M. J., Bodas, R., Bartolomé, D., Posado, R., García, J. J., & Olmedo, S. (2013). Agua electrolizada como higienizante en producción animal: Efectos en sanidad y productividad. Archivos de Zootecnia, 62, 13–23. https://doi.org/10.21071/az.v62irev.1954.
Unión Nacional de Avicultores (UNA). (2020). Indicadores económicos. Revisado de https://una.org.mx/indicadores-economicos/ Accesado el 23 de enero de 2020.
Wellman-Labadie O., Picman J. & M. Hincke. (2014). Actividad antimicrobiana de extractos proteicos de cutícula y cáscara externa de tres especies de aves doméstica. https://doi.org/10.1080/00071660802001722.