Número:
- Vol. 3
- Num. 18
- Noviembre - Diciembre
Ganaderia.com
Autores:
 Francisco Javier
Francisco Javier Vera Vázquez
Nacionalidad: Mexicana
Grado académico: Maestría en Ciencias en Recursos Genéticos y Productividad- Ganadería
ISSN-e:
2992-7293
Diseño de partículas de pectina protegida con aditivos poliméricos: mitigación de la degradación en el rumen y disminución del color amarillo de la leche de vacas en pastoreo
Introducción
La leche de vaca contiene β-caroteno, que es el compuesto responsable de la coloración amarillo-pálida, el color es un factor que se considera una medida visual de frescura y calidad (Khliji et al., 2010). La pectina es un polisacárido compuesto por ácido galacturónico que tiene la capacidad de disminuir la digestión de los carotenoides cambiando el entorno digestivo, ya que los carotenoides se digieren y absorben junto con los lípidos, al unirse con el calcio, interactúan con las sales biliares, alteran la viscosidad del medio digestivo, cambian la interfaz entre las fases de aceite y agua e inhiben la actividad de la lipasa pancreática (Cerón et al., 2019). Los microorganismos ruminales limitan la acción de aditivos, como la pectina, que requieren realizar su acción a nivel intestinal; por lo tanto, es necesario protegerlos para obtener mejor eficacia en la absorción, no toxicidad y precio (Peres et al 2016). El uso de polímeros sintéticos ha garantizado la integridad de los aditivos; sin embargo, una desventaja de los polímeros es el alto costo, éstos deben provenir de fuentes económicas y que sean de fácil disponibilidad para ser usados en el proceso de protección por lo que el objetivo de este estudio fue desarrollar un método económico para proteger pectina cítrica mediante la utilización de combinaciones de materiales protectores como aceite de palma, óxido de calcio y goma laca (un polímero natural). El estudio se llevó a cabo en dos fases: la primera fase implicó la elaboración y caracterización de las partículas de pectina cítrica, mientras que la segunda fase comprendió un experimento in vivo realizado con vacas en pastoreo.
Metodología
Cuatro novillos Holstein (300 ± 10.5 kg) fueron cuidados de acuerdo con los lineamientos del Consejo Mexicano de Cuidado Animal, y los procedimientos de cánula ruminal y duodenal se realizaron mediante cirugías tres meses antes del inicio del experimento. El protocolo para el mantenimiento y manejo de los novillos fue aprobado por el Comité Asesor Administrativo de Cuidado Animal del Colegio de Postgraduados, protocolo de estudiantes con matrícula 11831011.
El análisis se dividió en dos etapas:
Etapa 1: Caracterización y análisis de las partículas, que incluyó tres fases de estudio:
Fase 1: Diseño de partículas de pectina recubiertas de biopolímeros con el objetivo de proteger la pectina, haciéndola insoluble en el rango de pH de 5,8 – 6,5, y facilitando la degradación del biopolímero a pH < 4 para mejorar su disponibilidad a nivel intestinal y su unión con carotenos.
Fase 2: Evaluación de la tasa de liberación de la pectina a pH < 4,0 mediante la cuantificación de ácidos urónicos. Este método indirecto cuantifica la pectina liberada del biopolímero degradado.
Etapa 2: Evaluación de las partículas de pectina protegida en el rumen y la productividad de las vacas, que incluye dos fases de estudio:
Fase 3: Evaluación de la degradación de las partículas de pectina protegida en bovinos a través de bolsas in situ introducidas en el rumen de bovinos canulados.
Fase 4: Desarrollo de un ensayo in vivo con vacas lactantes en pastoreo, evaluando metabolitos sanguíneos y características fisicoquímicas de la leche.
Fase 1: Las partículas se elaboraron utilizando pectina cítrica (grado de esterificación 69%). Los encapsulantes utilizados fueron aceite rojo de palma africana (Elaeis guinnensis), óxido de calcio, goma laca blanca en polvo, alcohol etílico grado reactivo (96°) y agua destilada.
El procedimiento se realizó con una modificación de la técnica descrita por Pablos en 2005. Primero se pesaron 100 g de aceite de palma y se calentaron ligeramente hasta alcanzar su punto de fusión a 50 °C. Después, se añadieron 100 g de pectina y se homogeneizó. Al aceite caliente se le añadió óxido de calcio (CaO) en una proporción 1:1. La mezcla se calentó adicionalmente entre 100-150 °C mientras se aplicaba una presión de 2 a 4 bares durante 20 minutos utilizando un autoclave. Simultáneamente, se añadieron 200 mL de agua destilada a la mezcla para permitir que el CaO formara CaOH. Este procedimiento fue el diseño de las partículas de pectina cítrica protegidas con aceite de palma (PwP). Posteriormente, las partículas de pectina cítrica secas se impregnaron con una solución de goma laca durante 5 minutos. La solución de goma laca se preparó mezclando 200 g de goma laca con 1 L de alcohol de grado reactivo y agitándola durante 20 minutos en una placa magnética, y se diseñaron como partículas de pectina cítrica protegidas con aceite de palma y goma laca (PwPL). Las partículas de pectina protegidas se secaron a temperatura ambiente durante 24 horas y se almacenaron en bolsas de plástico de 10 kg. Las partículas protegidas se caracterizaron mediante microscopía electrónica de barrido. Las muestras se colocaron en un portamuestras de latón y se aseguraron con cinta de aluminio de doble adhesivo y cinta conductora de carbono de doble adhesivo. Las partículas fueron recubiertas con oro durante 4 minutos utilizando un ionizador de metales. Posteriormente, las muestras fueron observadas y analizadas en un microscopio electrónico de barrido a 10 Kv.
Fase 2: Las soluciones tampón (pH 7 y 5) se prepararon mezclando bicarbonato de sodio (Fermont 12903-2,5), fosfato de sodio heptahidratado (J.T. Baker 3828-01), cloruro de potasio (KCl) (J.T.Baker 3040-1), cloruro de sodio (NaCl) (Meyer 2365-500) y sulfato de magnesio heptahidratado (J.T.Baker 2500) en 2 L de agua destilada. La saliva artificial de McDougall se ajustó a un pH de 7,0 a 5,0 utilizando ácido acético (J.T.Baker 9507-60). Además, el tampón de pH 3,0 se preparó mezclando 10,21 g de ftalato ácido de potasio (Mallinckrodt 5704) con 250 mL de agua y 4,108 mL de ácido clorhídrico (HCl) (J.T.Baker 9535-05), y completando el volumen a 250 mL. Para crear el tampón de pH 2,0, se mezclaron 3,73 g de KCl con agua destilada para alcanzar un volumen de 250 mL. Luego, 100 mL de la solución de KCl se mezclaron con 21,2 mL de la solución de HCl y el volumen se ajustó a 400 mL para las pruebas de degradabilidad.
Las pruebas de velocidad de liberación se dividieron en tres tratamientos: PnP (que involucró pectina cítrica sin protección), PwP y PwPL. Se prepararon diez réplicas de cada tratamiento utilizando 0,5 g de muestra en un tubo plástico de 50 mL. Posteriormente, se añadieron 25 mL de cada solución tampón (pH: 2, 3, 5, 7) a los tubos, que luego se colocaron en un frasco de vidrio en el digestor Daisy Ankom a una temperatura de 39 °C para simular las condiciones del rumen. Las muestras se agitaron continuamente. Después de 1 hora, se tomó una alícuota de 250 µl de cada muestra y se colocó en un baño de hielo sobre una placa magnética para la digestión ácida. Luego, cada muestra se trató con 1 mL de ácido sulfúrico concentrado (H2SO4) y se agitó magnéticamente durante 10 minutos. A continuación, se añadieron 500 µL de agua destilada a cada muestra y se agitó durante 10 minutos. Este proceso se repitió añadiendo otros 500 µL de agua destilada y agitando durante 20 minutos. Finalmente, las muestras se agitaron y se enfriaron con hielo durante 10 minutos antes de medir la concentración de ácidos urónicos.
Cuantificación de ácidos urónicos: Se colocó una alícuota de 0,1 mL de cada muestra en un baño de hielo y se añadió 1 mL de una solución al 0,5% de borato de sodio en H2SO4 concentrado. La mezcla resultante se agitó en un mezclador y se colocó en agua hirviendo (100 °C) durante 5 minutos. Luego, los tubos se enfriaron en hielo durante 5 minutos y se agregaron 20 µL de m-fenilfenol al 0,15% en hidróxido de sodio al 0,5%. Después de agitar, los tubos se dejaron a temperatura ambiente (24 - 27 °C) durante 15 minutos. Después del período de reposo, las muestras se agitaron y se midió la absorbancia a 520 nm utilizando un espectrofotómetro. La concentración se calculó mediante una curva de calibración que oscilaba entre 0 y 40 µg de ácido D-galacturónico (Sigma All-drich). La pectina liberada en las partículas protegidas se determinó calculando el porcentaje de ácidos urónicos mediante la siguiente fórmula:

Fase 3: Se utilizaron tres toros Holstein con un peso vivo de 500 ± 50 kg, equipados con fístulas y cánulas ruminales. Los tratamientos evaluados fueron los siguientes: a) PnP, b) PwP y c) PwPL, a dos tiempos de degradabilidad, 24 y 48 horas. Para cada tratamiento, se colocaron 20 gramos de muestra en una bolsa de tela tipo polyseda (nylon®) de 10 x 20 cm con un tamaño de poro de 115 μm. Posteriormente, estas bolsas se introdujeron al rumen a través de la cánula. Cada tratamiento contó con 5 réplicas y se utilizaron dos bolsas adicionales como blanco, dando como resultado un total de 34 bolsas para cada animal. Después de la incubación en el rumen, las bolsas se retiraron y se lavaron con agua corriente. Posteriormente, se secaron en una estufa a 50 °C durante 24 horas. El porcentaje de degradabilidad de la pectina protegida se calculó utilizando la siguiente fórmula:

Donde:
Degradabilidad de la materia seca in situ = Degradabilidad de la materia seca in situ de PnP, PwP o PwPL
MS inicial y residual = Materia seca inicial y residual de PnP, PwP o PwPL
Fase 4: El diseño de este experimento se planteó con los resultados obtenidos en la fase 2 y 3. Los resultados sí muestran diferencias entre las dos técnicas de encapsulación de pectina. Sin embargo, se seleccionó PwPL para su uso en la unidad experimental animal. En consecuencia, se utilizaron 20 vacas para el experimento, las cuales fueron cruces entre cebú y suizo. Las vacas tenían un peso medio de 400 ± 50 kg y eran multíparas. Estaban en pastoreo extensivo y tenían acceso a pasto colocho (Digitaria swazilandensis) y agua ad libitum. Las vacas se dividieron aleatoriamente en dos grupos, con 10 animales en cada grupo. Los tratamientos administrados fueron los siguientes: NP, que no incluía pectina cítrica, y PwPL, que consistió en proporcionar 100 g de pectina cítrica protegida por animal por día. Las partículas de pectina se mezclaron con 250 g de concentrado comercial y se ofrecieron a las vacas después del ordeño (7:00 am). El experimento duró un período de 45 días.
Ordeño y toma de muestra de leche: Las vacas fueron ordeñadas manualmente a las 7:00 am. Dos veces por semana, se recogió una muestra de 100 mL de leche por vaca en botellas plásticas de 120 mL y se almacenó a -4 °C hasta su análisis. Previo al análisis, las muestras fueron descongeladas a temperatura ambiente y luego calentadas a 30 ºC utilizando un baño maría. Posteriormente, las muestras fueron transferidas a un matraz de 250 ml y homogeneizadas. Se tomó una porción de 15 mL de la muestra y se colocó en el portamuestras de un analizador de leche digital. Después de un tiempo de duración de 60 segundos, se registró el porcentaje de grasa, proteína, sólidos totales, lactosa y pH. El color de la leche se midió utilizando un colorímetro de precisión, que registró los valores de CIEL* (luminosidad), a* (índice rojo), b* (índice amarillo) y los valores del índice de saturación C (croma, C*). El valor C* se define por el ángulo entre a* y b* y se denota como (a2+b2)1/2. Los grados Brix se cuantificaron utilizando un refractómetro.
Toma de muestras y análisis de sangre: Las muestras de sangre se recogieron el último día del experimento, 2 horas después de la alimentación, puncionando la vena coccígea con agujas y tubos de plástico de 6 mL que contenían heparina sódica. Posteriormente, se cuantificaron los metabolitos sanguíneos, incluyendo glucosa, colesterol, triglicéridos y lactato, utilizando un medidor portátil.
Análisis estadístico
Etapa 1: Las partículas de pectina cítrica fueron sometidas a caracterización microscópica cualitativa. Los datos obtenidos del ensayo de liberación in vitro, que midió la liberación de pectina en forma de ácido D-galacturónico, fueron analizados mediante el procedimiento SAS GLM con un diseño completamente al azar. Las medias entre tratamientos fueron comparadas mediante la prueba de Tukey (p<0,05).
Etapa 2: Los datos de degradación in situ de las partículas fueron analizados mediante un diseño completamente al azar con el procedimiento PROC ANOVA de SAS. Las medias entre tratamientos fueron comparadas mediante la prueba de Tukey (p<0,05). Los datos correspondientes a las características fisicoquímicas de los metabolitos de la leche y la sangre fueron analizados mediante un diseño completamente al azar con dos tratamientos y diez repeticiones. La comparación entre tratamientos se realizó mediante la prueba t-Student (p<0,05).
Resultados
Fase 1
Partículas de pectina recubiertas de biopolímeros. La figura 1 muestra la morfología de las PwP. Se observan partículas de diferentes formas y tamaños (desde 70 hasta >300 µm).

La Figura 2 muestra las partículas de pectina cítrica protegidas con aceite de palma y óxido de calcio, la forma y superficie de estas fueron similares a las partículas de pectina a las que se le proporcionó recubrimiento con goma laca por inmersión, con tamaños de 70 a 200 µm. La superficie de las partículas también presentó algunas manchas blancas, esta característica puede deberse a la acumulación de iones de calcio formando manchas blancas en la película de las partículas.

La figura 3 muestra la morfología de PwPL por inmersión. La superficie de las partículas estaba mejor compactada, lo que indica una buena funcionalidad de la película de goma laca.

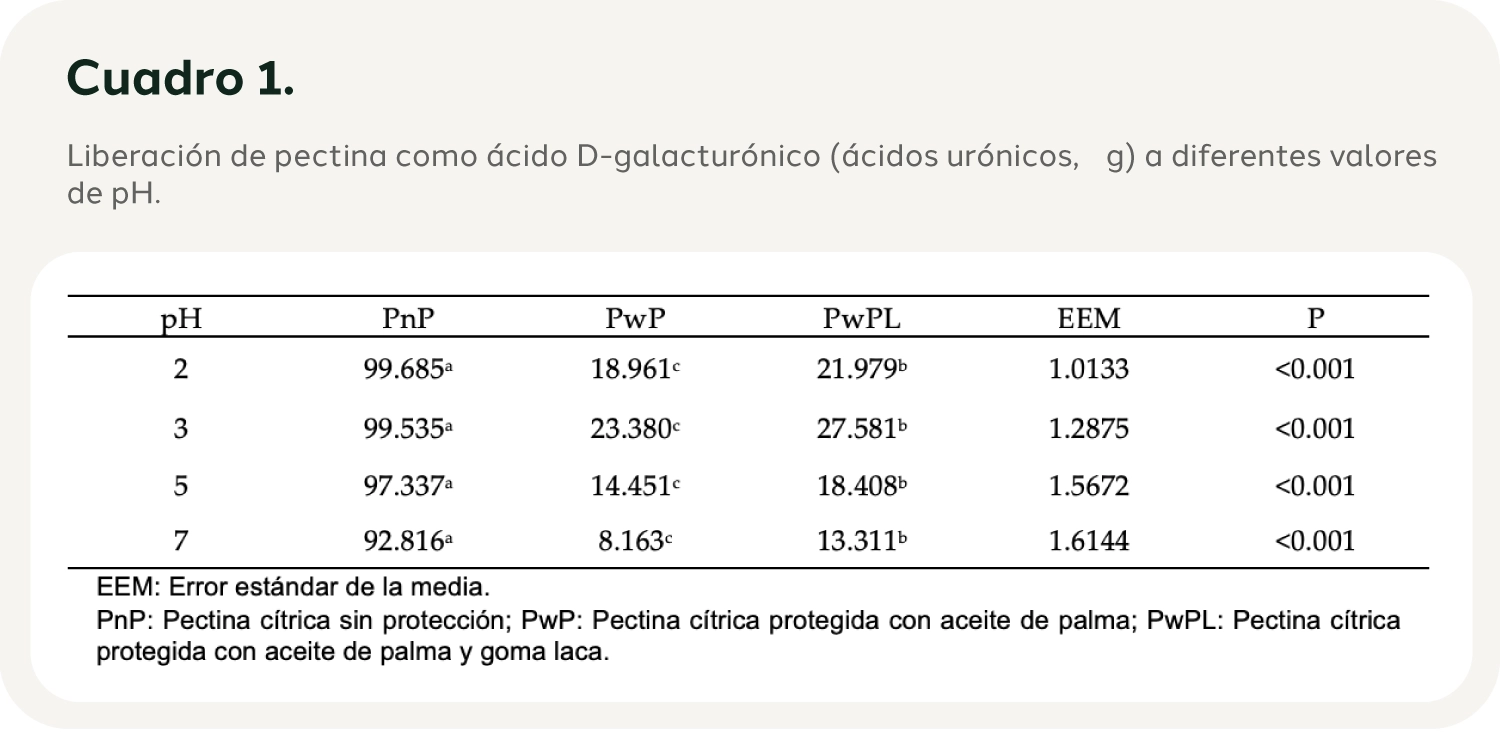
Tasa de secreción de pectina evaluada a diferencias de pH: La liberación de ácido D-galacturónico (ácidos urónicos, µg) fue mayor a pH 3,0 en los tratamientos (P<0,05). En las soluciones de pH 2, 5 y 7, los valores de ácido D-galacturónico se liberaron en baja cantidad. El PwPL tuvo mayor liberación de ácidos urónicos (P<0,01) que el PwP (Cuadro 1).
Fase 2
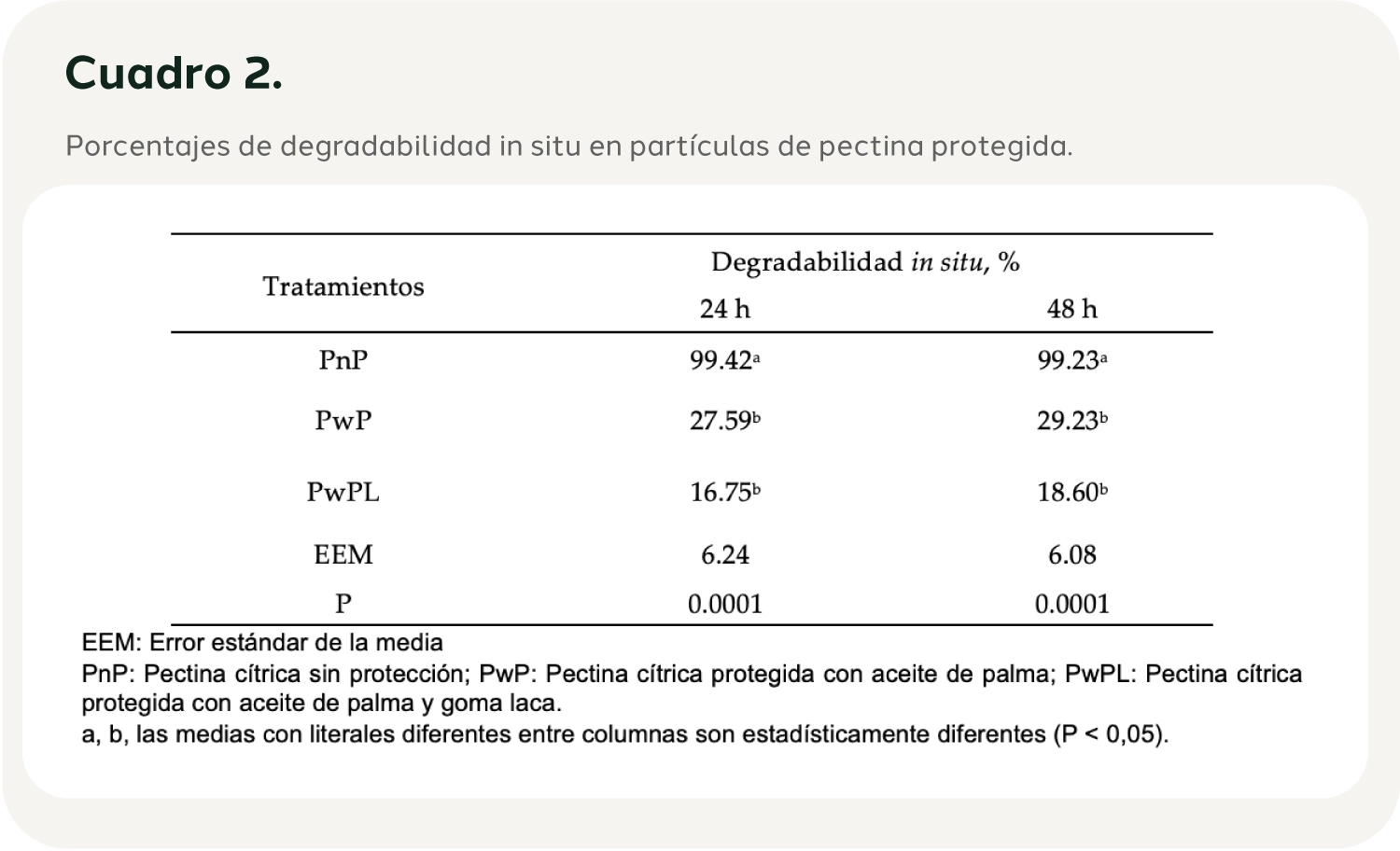
Degradabilidad in situ de la pectina con dos técnicas de protección. El porcentaje de degradabilidad in situ de la pectina cítrica protegida con las dos técnicas evaluadas presentó diferencias (P<0,05). La pectina cítrica desprotegida (PnP) se degradó en un 99% a las 24 y 48 horas, mientras que la PwP fue de 27,59% a las 24h y 29,23% a las 48h. La protección por inmersión con goma laca, PwPL, presentó una menor degradabilidad a las 24 y 48 h de incubación de 16,75% y 18,60%, respectivamente (Cuadro 2).
Se realizó un ensayo in vivo con vacas lactantes en pastoreo, evaluándose algunos metabolitos sanguíneos y características fisicoquímicas de la leche.
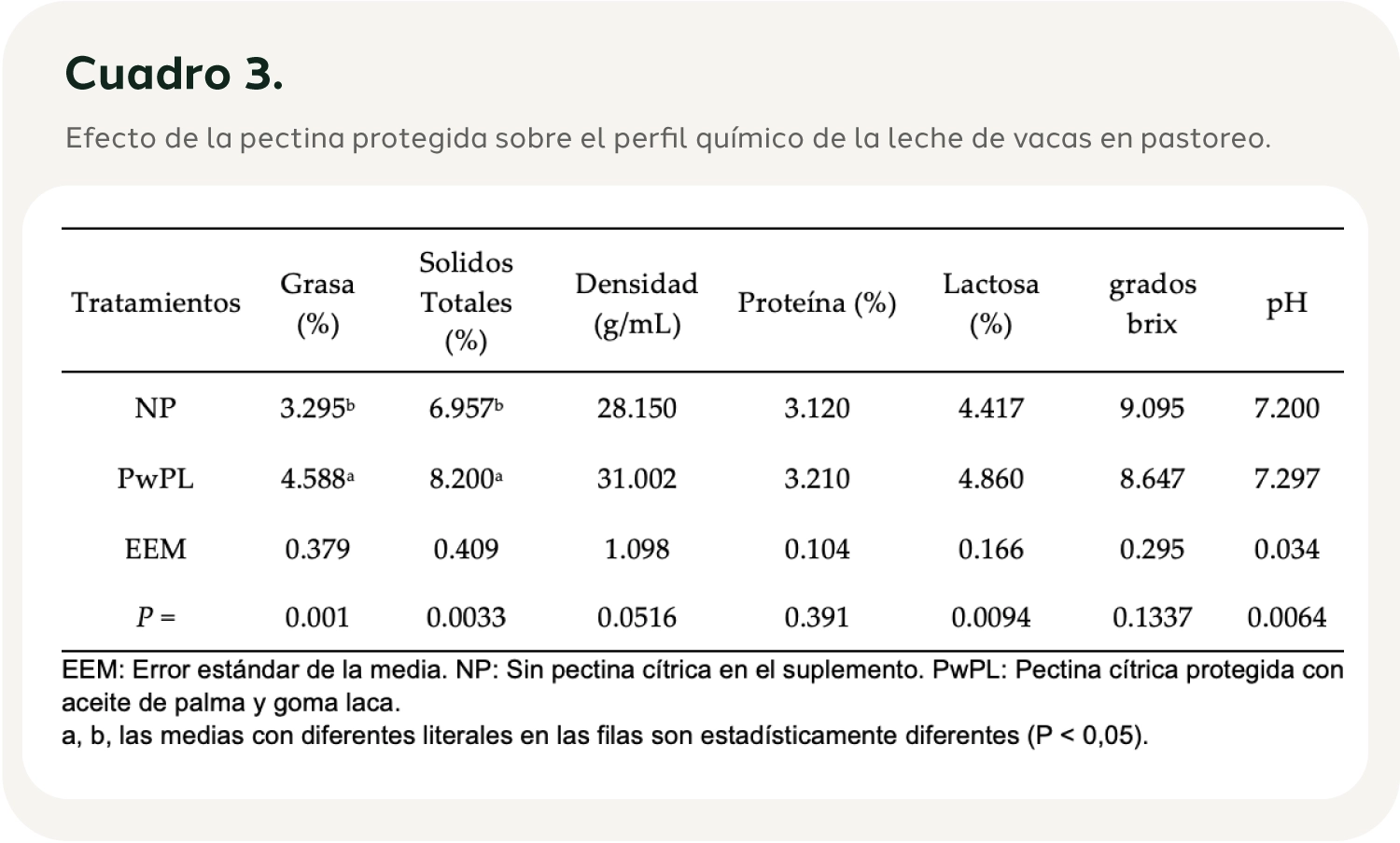
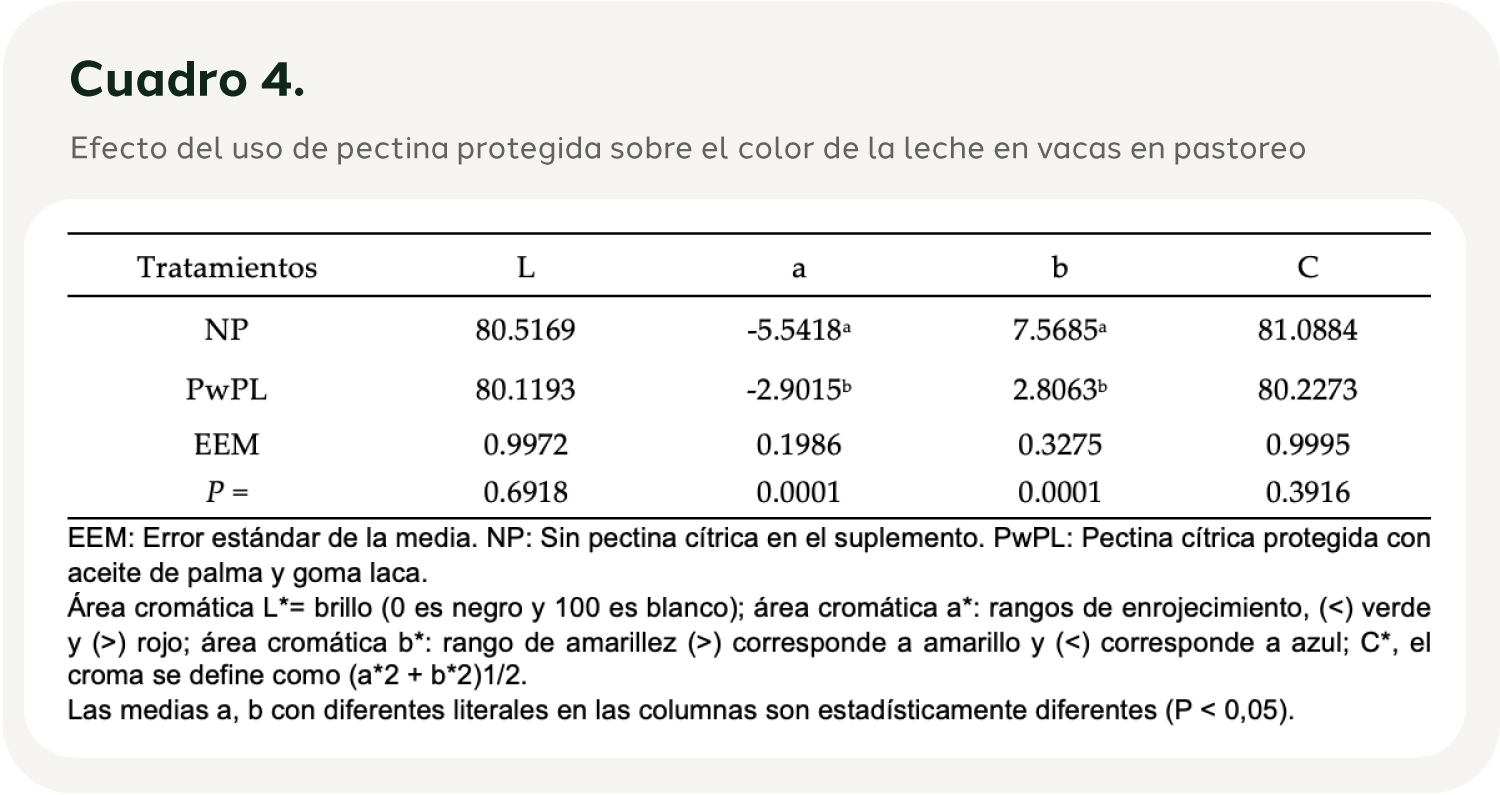
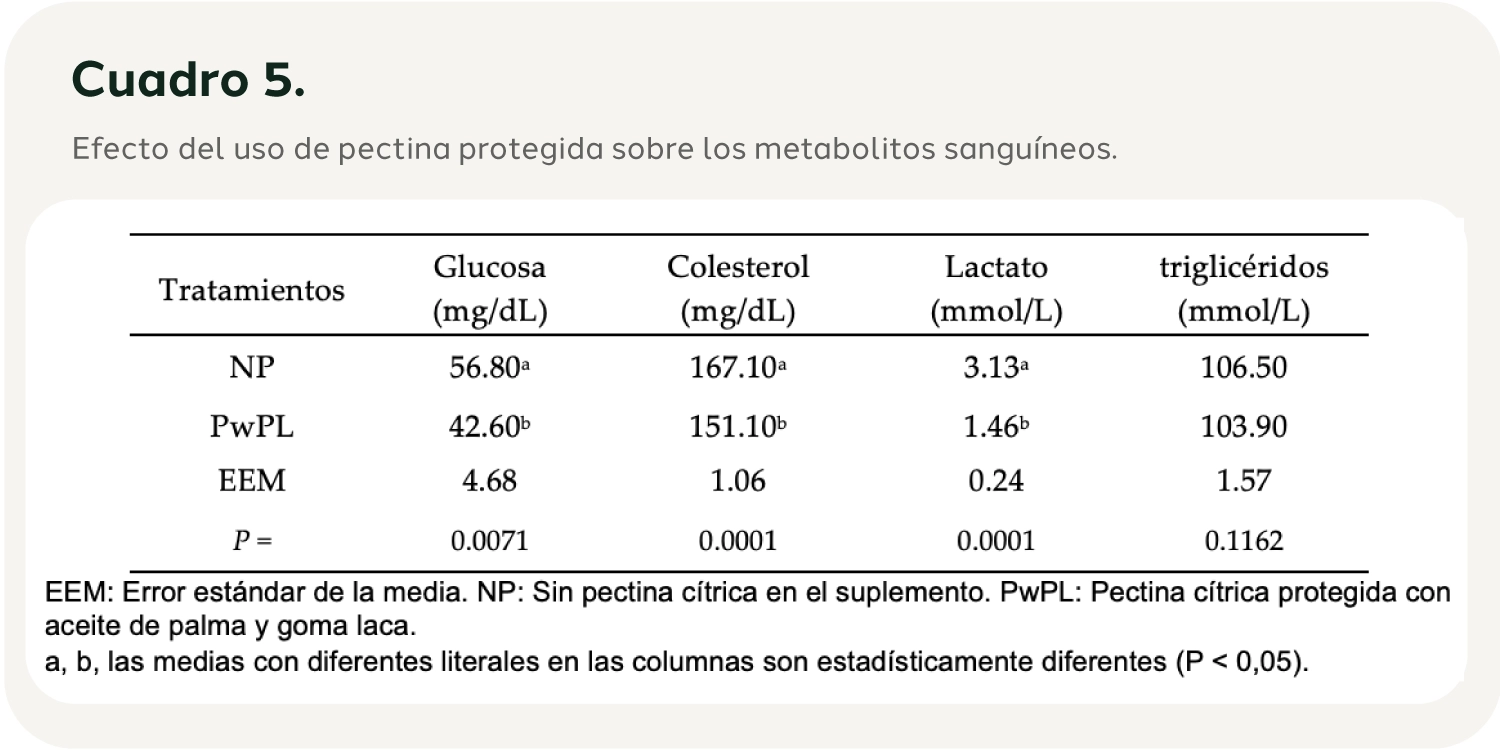
Efecto del uso de pectina protegida sobre el perfil químico de la leche de vacas en pastoreo: El uso de pectina cítrica protegida en la alimentación de vacas lecheras incrementó (P<0.05) el porcentaje de grasa en la leche (4.588 vs. 3.295%). Los sólidos totales aumentaron 17% con el uso de pectina protegida (8.2 vs. 6.96%). Los tratamientos no presentaron diferencias en contenido de proteína, densidad, grados brix y pH (Cuadro 3). La pectina cítrica protegida en la alimentación de vacas presentó un valor L* similar en los dos tratamientos. El valor a* (NP=-5.5418, PwPL =-2.9015) y el valor b* (NP=7.5685, PwPL =2.8063) presentaron diferencias significativas (P<0.05), mientras que el valor c* no presentó diferencia significativa (P >0.05) (Cuadro 4). La pectina cítrica protegida en vacas lecheras disminuyó (P < 0,05) la concentración sanguínea de glucosa (NP = 56,80 vs. PwPL = 42,60 mg dL-1), colesterol (NP = 167,10 vs. PwPL = 151,10 mg dL-1) y lactato (NP = 3,13 vs. PwPL = 1,46 mg dL-1). No hubo diferencias en los niveles de triglicéridos en sangre (Cuadro 5).
Discusión
La liberación lenta de partículas, elaboradas con polímeros, está influenciada por varias características endógenas y exógenas. Estas características incluyen tamaño de partícula, morfología, porosidad, higroscopicidad, hidrofobicidad, tensión superficial y acción térmica (Choudhury et al., 2021). Sin embargo, al diseñar partículas específicamente para su degradación en el tracto digestivo de rumiantes, es esencial centrarse en los factores que facilitan la liberación de fármacos o aditivos. En este caso, la sensibilidad al pH es la variable principal que influye en la degradación de partículas (Del Piano et al., 2011), y se puede controlar a través del recubrimiento de polímeros. En nuestro estudio, las partículas de pectina protegidas con aceite de palma y goma laca (PwPL) demostraron un rendimiento satisfactorio, degradándose dentro del rango de pH de 3 a 5. Estudios similares han protegido con éxito otras sustancias, como Lactobacillus plantarum y ácidos grasos omega-3, utilizando alginato y pectina (López et al., 2019), o empleando goma laca como material de recubrimiento en la producción de microcápsulas de resina de urea-formaldehído (Wang et al., 2022).
El color de la leche está influenciado por varios factores extrínsecos e intrínsecos, siendo la dieta, la cantidad de glóbulos de grasa y el almacenamiento de pigmentos los que tienen un impacto significativo, el color sirve como un método eficaz de trazabilidad, permitiendo la determinación del sistema de alimentación de la vaca, y está asociado con la calidad de la leche (Prache, 2007). En nuestro estudio, las partículas de pectina protegidas disminuyeron el valor *b, que está asociado con el grado de coloración amarilla en la leche. Nuestros resultados indican que la pectina es un antagonista eficaz de los β-carotenos, evitando su absorción, acumulación en la glándula mamaria y posterior excreción en la leche (Cruz et al., 2007). Los niveles de colesterol, glucosa y lactato encontrados en las vacas en este estudio coinciden con investigaciones previas realizadas por nuestro grupo de investigación. El estudio indica que los niveles de colesterol hemático en terneros disminuyeron en un 15, 18 y 27% a medida que la dosis de pectina aumentó de 18,5 a 46,25 y 92,5 g/día.
Conclusión
El diseño de partículas protegidas con lípidos y polímeros es un método económico que resiste la degradación a niveles de pH superiores a 5. Las partículas diseñadas exhibieron formas irregulares, rugosas y porosas, siendo la morfología y la textura dependientes del polímero utilizado. Estas partículas protegidas fueron utilizadas de manera efectiva en rumiantes. Por ejemplo, la inclusión de 100 g de pectina por animal por día en el alimento de vacas lecheras en pastoreo resultó en una reducción de la coloración amarilla de la leche, y las características fisicoquímicas de la leche permanecieron inalteradas.
Bibliografía
Aguiar., Z, E., Rojas., B, A., & Murillo., B, J. (2022). Efecto de la suplementación de β-caroteno en vacas lecheras sobre concentraciones en sangre y calostro, reproducción y salud de la ubre. Nutrición Animal Tropical, 16(1), 53-81.
Cerón, G. T., Bribiesca, J. E. R., Jiménez, L. M., Monterrosa, R. G. C., Mancera, H. A. Z., Galván, M. M. C., ... & Sánchez, D. H. 2019. Design of Pectin Microcapsules Protected with Shellac and Sodium Alginate with Sensibility of Degradation in Intestinal pH of Bovine. REV.CHIM.(Bucharest). 70(12): 4233-4237.
Choudhury N, Meghwal M, & Das K. (2021) Microencapsulation: An overview on concepts, methods, properties and applications in foods. Food Frontiers. 2(4):426-442. Doi. 10.1002/fft2.94.
Cruz, M., R.G., Ramirez, B., J. E., Guerrero, L., M. I., y Zinn, R., A. (2015). Influence of Pectin on Intestinal Digestion of Chromogens in Steers. Anim. Feed Sci. Technol. (207): 274-77. doi:org/10.1016/j.anifeedsci.2015.06.015
Del Piano, M., Carmagnola, S., Ballarè, M., Sartori, M., Orsello, M., Balzarini, M, Pagliarulo, M., Tali, R., Anderloni, A., Strozzi, G.P., Mogna, L., Sforza, F. & Capurso, L. (2011). Is Microencapsulation the Future of Probiotic Preparations. The Increased Efficacy of Gastro-Protected Probiotics. Gut Microbes 2(2): 120-23. doi.org/10.4161/gmic.2.2.15784.
Khliji, S., van de Ven, R., Lamb, T. A., Lanza, M., y Hopkins, D. L. (2010). Relationship between consumer ranking of lamb colour and objective measures of colour. Meat Sci. 85(2): 224-229. doi: 10.1016/j.meatsci.2010.01.002
López-Fernández, S. G., Michel, S. G. F., Corral, R. I. A., García-Galaz, A., Moreno-Rivas, S. C., Vázquez-Moreno, L., & Montfort, G. R. C. (2019). Caracterización del co-encapsulamiento de Lactobacillus plantarum y ácidos grasos omega-3 en una matriz de alginato-pectina. Biotecnia, 21(2), 38-46.
NORMA Oficial Mexicana NOM-062-ZOO-1999, Especificaciones técnicas para la producción, cuidado y uso de los animales de laboratorio. Pp 107-165.
Pablos, P., E. (2005). Procedimiento de fabricación de jabones cálcicos para alimentación animal. Patente WO2007077266A1. Fecha de publicación: 12 de julio de 2007. Pp 1-18.
Peres, L. B., de Araújo, P. H. H., & Sayer, C. (2016). Solid lipid nanoparticles for encapsulation of hydrophilic drugs by an organic solvent free double emulsion technique. Colloids Surf. B. (140): 317-323. doi: 10.1016/j.colsurfb.2015.12.033.
Prache S. (2007). Developing a diet authentication system from the composition of milk and meat in sheep: a review. J Agri Sci. 145: 435–444. Doi 10.1017/S0021859607007174
Wang, L., Han, Y., & Yan, X. (2022). Effects of adding methods of fluorane microcapsules and shellac resin microcapsules on the preparation and properties of bifunctional waterborne coatings for basswood. Polymers, 14(18), 3919.