Número:
- Vol. 3
- Num. 18
- Noviembre - Diciembre
Porcicultura.com
Autores:
 Perla Lucero
Perla Lucero Zavala Ocampo
Nacionalidad: Mexicana
Grado académico: Ingeniero biotecnólogo
 José Luis
José Luis Cerriteño Sánchez
 Julieta Sandra
Julieta Sandra Cuevas Romero
ISSN-e:
2992-7293
Construcción de un sistema de expresión de la proteína P30 y P72 del virus de la Peste Porcina Africana (VPPA)
Perla Lucero Zavala Ocampo1,2 ; José Luis Cerriteño Sánchez1; Julieta Sandra Cuevas Romero1
1Centro Nacional de Investigación Disciplinaria en Salud Animal e Inocuidad, INIFAP. Carretera México-Toluca, KM 15.5, Palo Alto. CDMX, México.
2Universidad Nacional Autónoma de México. Posgrado en Ciencias de la Producción y de la Salud Animal.
Resumen
La peste porcina africana es una enfermedad extremadamente contagiosa, de naturaleza aguda y severa con síntomas hemorrágicos, que impacta a los cerdos de granja y a los jabalíes, siendo provocada por el virus de la peste porcina africana (VPPA). El objetivo de este trabajo es establecer las bases para el desarrollo de métodos de diagnóstico como herramientas para la detección temprana y a gran escala de la peste porcina africana que puedan utilizarse en un laboratorio con nivel de bioseguridad 2 en México, mediante la clonación de genes y análisis de las proteínas p30 y p72 del vPPA. La presente investigación consistió en el análisis bioinformático y la caracterización in silico de las proteínas p72 y p30 del VPPA con base en la aplicación de herramientas biotecnológicas y la amplificación de genes para la generación de un sistema de expresión recombinante. Se hizo una revisión de la antigenicidad de cada proteína y el diseño de oligonucleótidos para amplificar la región proteica apropiada para la clonación y expresión de manera recombinante en el vector de expresión de pET SUMO. En este trabajo, se logró estudiar las características de las proteínas p30 y p72, así como amplificar genes derivadas de dichas proteínas para generar un sistema de expresión recombinante que permitirán proponerlas para su uso en el desarrollo de sistemas diagnósticos eficientes y oportunos contra la peste porcina africana. Debido al peligro potencial que representa esta enfermedad para el país.
Palabras clave: peste porcina africana, p72, p30, cerdos, recombinante.
Introducción
La peste porcina africana es una enfermedad altamente infecciosa aguda, grave y hemorrágica (tasa de mortalidad y morbilidad cercana al 100%) que afecta a cerdos domésticos y silvestres y es causada por el virus de la peste porcina africana (VPPA) (Wu et al. 2022). Actualmente se han caracterizado antígenos del VPPA para obtener información relevante que ayude a incrementar el control y erradicación de la enfermedad. Un ejemplo son las proteínas p30 (CP204L) y p72 (B646L) las cuales son proteínas de superficie del VPPA que inducen anticuerpos neutralizantes en cerdos (Zhang et al. 2022). Específicamente, las proteínas p30, pp62, p72 y CD2v están involucradas en la respuesta inmune de las células T de los cerdos vivos infectados con VPPA, entre las cuales las proteínas p72 y pp62 son las que tienen respuestas inmunitarias humorales y de células T específicas más fuertes (Sun et al. 2021). Además, estudios previos muestran que la inmunización con una combinación de p30 y p54 recombinantes, o una proteína quimérica p54/30, indujo respuestas de anticuerpos eficaces en cerdos y logró diferentes grados de protección contra la exposición a VPPA (Zhang et al. 2022). La presencia de la PPA en República Dominicana desde el reporte del primer brote en 2021 representa una amenaza latente para México, que deriva en la necesidad de detección oportuna de los animales infectados y serológicamente positivos, basado en la aplicación de herramientas biotecnológicas, como el uso de proteínas recombinantes del virus. Con esto, p72 y p30 se convierten en proteínas para tener en cuenta para investigaciones que evalúen su potencial uso en el desarrollo de pruebas diagnósticas a través del desarrollo de sistemas imunoenzimáticos como el iELISA, de tal manera que forme parte de las medidas de combate de esta enfermedad y se minimicen las consecuencias económicas en el país. Por lo que este trabajo tiene la finalidad de establecer las bases para el desarrollo de métodos de diagnóstico como herramientas para la detección temprana y a gran escala de la peste porcina africana que puedan utilizarse en un laboratorio con nivel de bioseguridad 2 en México, mediante la clonación de genes y análisis de las proteínas p30 y p72 del vPPA, así como el análisis bioinformático y caracterización in silico de las proteínas p72 y p30, además de amplificar los genes mediante una estrategia recombinante para la generación de un sistema de expresión que pueda ser utilizado en un futuro como una herramienta de diagnóstico de la enfermedad.
Material y métodos
Para este estudio se trabajó con la secuencia del genoma reportado de la peste porcina africana aislado en Georgia en 2007 (No. Acceso en GenBank FR682468), usado como cepa de referencia para México. Se diseñaron oligonuclétidos específicos para amplificar los ORFs de las proteínas p30 y p72, las cuales han sido usadas en otras partes del mundo debido a su grado de conservación y capacidad para generar respuesta inmune. Se llevó a cabo la amplificación de p30 y p72 a partir de cDNA de la cepa Georgia 2007, mediante gradiente de temperaturas en PCR punto final. Los productos de clonación fueron secuenciados mediante SANGER y las secuencias fueron analizadas mediante el paquete bioinformático de DNAstar y los árboles filogenéticos se realizaron utilizando la máxima verosimilitud basada en el modelo JTT y distribución Gamma con al menos 1000 réplicas utilizando el software MEGA X. Posteriormente a partir de genes sintéticos derivados del genoma reportado de la peste porcina africana aislado en Georgia en 2007, con número de acceso: FR682468, que contiene las proteínas p72 y p30 fueron empleadas como molde para el desarrollo de este proyecto, las cuales han sido usadas en otras partes del mundo debido a su grado de conservación y capacidad para generar respuesta inmune. Swiss Model fue utilizado para la predicción del peso molecular y la estructura de ambas proteínas. Se obtuvo un modelo propuesto basado en la estructura de la proteína p72 y p30 con un porcentaje de homología mayor al 30%. Posteriormente, con el paquete bioinformático DNASTAR se realizó el análisis de las secuencias proteicas. Para la revisión de la antigenicidad se usaron los algoritmos de Jameson-Wolf (1988) y Kolaskar y Tongaonkar (1990) se usaron para predecir los sitios antigénicos y seleccionar la región proteica apropiada para la expresión en E. coli. Kyte y Doolittle (1982) se utilizaron para evaluar los residuos hidrofílicos e hidrofóbicos a lo largo de la secuencia de aminoácidos de las proteínas. La probabilidad de que una región de proteína dada se encuentre en la superficie se evaluó utilizando el enfoque de Emini et al. (1985). Los sitios glicosilados se predicen usando NetNGlyc - 1.0. Por otro lado, se diseñaron oligonucleótidos específicos usando Oligo Analyzer de IDT para recuperar el gen correspondiente al fragmento predicho como el mejor candidato a expresión correspondiente a una porción del N-terminal de p72 y la región completa de p30, finalmente se propone un sistema de expresión recombinante para estas regiones, y su detección en un peso molecular esperado de 42 kDa kDa (p72) y 33 kDa (p30). Para comprobar la temperatura más adecuada de reacción de PCR se realizó un gradiente de temperaturas mientras que, para verificar la presencia y amplificación adecuada de las proteínas, se realizaron reacciones de PCR y electroforesis en gel de agarosa al 1%. Para la producción de las proteínas, se indujeron cultivos de expresión en medio LB con IPTG en el sistema de E. coli como vector de expresión. Finalmente, la presencia de las proteínas recombinantes se corroboró mediante SDS-PAGE y Western blot usando anticuerpos anti-his. Los cuerpos de inclusión (obtenidos por ruptura mecánica) solubilizados se purificaron usando una columna de agarosa Ni-NTA. Las proteínas fueron liofilizadas y se cuantificaron con el método de Bradford para obtener el rendimiento correspondiente para su uso posterior.
Resultados y discusión
Análisis bioinfomático
El análisis bioinformático de la secuencia nucleotídica y proteica de Georgia 2007 p30 y p72, mostró que este aislamiento se encontraba dentro del genotipo II del virus de PPA, en el mismo genogrupo de las secuencias reportadas durante los últimos brotes de PPA, en los últimos 10 años incluyendo República Dominicana 2021, mostrando una homología del 100% (Figura 1). El análisis bioinformático de la secuencia nucleotídica y proteica de Georgia 2007-p30 indicó un 97.85% encontraba dentro del genotipo II (Figura 1).

Caracterización in silico de la antigenicidad de la proteína p72
La secuencia completa de la proteína p72 está conformada por 646 residuos de aminoácido y un peso de 73.155 kDa. El fragmento de proteína presenta un peso de 28.651 kDa con 254 residuos de aminoácido, comienza con el ácido glutámico (Glu, E) en el residuo 73 y termina con prolina (Pro, P) en el residuo 326, seleccionada de la región N-terminal con el mayor índice de antigenicidad, de probabilidad de superficie, con regiones hidrofílicas, con presencia de 10 determinantes antigénicos (epítopos) y 1 sitio glicosilado (Figura 2).
Como se observa en la Figura 2, se obtuvo un modelo propuesto basado en la estructura de la proteína p72 con un porcentaje de homología mayor al 30% (97.64%), donde se predice una estructura circular, con ~14 colas y estructura secundaria de ~9 hélice alfa. De los logaritmos se observó una alta hidrofilicidad en la región proteica, lo que permite una mayor solubilidad de la proteína, con una probabilidad de superficie de 3, con 14 regiones antigénicas, 10 epítopos y la predicción de un sitio glicosilado (señalado con una flecha color rojo). Con el análisis de los residuos hidrofílicos e hidrofóbicos a lo largo de la secuencia, la probabilidad de superficie y antigenicidad se pudo seleccionar una región del extremo N-terminal de la proteína p72 como una proteína antigénica que contiene los epítopos más inmunogénicos y mejores candidatos para clonación y expresión de manera recombinante en el vector pET SUMO. Posteriormente, se diseñaron un par de oligonucleótidos que amplifiquen este fragmento de proteína, donde las secuencias 5'- GAA TAC AAT AAA GTA CGC CCG CAT ACG -3' y 5'- CTA CTA AGG GGG CTG ATA GTA TTT AGG GGT -3' corresponden al oligonucleótido forward y reverso, respectivamente. Para ambos cebadores, todos los valores de ΔG en la formación de horquillas y autodímeros son mayores a -5 (no significativos), con un porcentaje de CG de 44.4 y 46.7%, y una diferencia de temperaturas de 2.2°C. La mejor temperatura de alineación fue la del carril 4 (67.6°C) (Figura 3).

Caracterización in silico de la antigenicidad de la proteína p30
Por otro lado, la secuencia completa de la proteína p30 está conformada por 194 residuos de aminoácido y un peso de 22.39 kDa. La proteína amplificada presenta un peso de 19.983 kDa con 174 residuos de aminoácido, comienza con el ácido glutámico (Glu, E) en el residuo 12 y termina con leucina (Leu, L) en el residuo 186, se analiza el índice de antigenicidad, de probabilidad de superficie y las regiones hidrofílicas de la región, con presencia de 7 determinantes antigénicos (epítopos) y 1 sitio glicosilado (Figura 4).
Como se observa en la Figura 4, en los logaritmos se observó una alta hidrofilicidad en la región proteica, lo que sugiere una mayor solubilidad de la proteína, con una probabilidad de superficie de 2, con 7 regiones antigénicas, 7 epítopos y la predicción de un sitio glicosilado (señalado con una flecha color rojo). Con el análisis de los residuos hidrofílicos e hidrofóbicos a lo largo de la secuencia, la probabilidad de superficie y antigenicidad se puede analizar la proteína p30 como una proteína antigénica que contiene epítopos inmunogénicos ideales para clonación y expresión de manera recombinante en el vector pET SUMO. Posteriormente, se diseñaron un par de oligonucleótidos que amplifiquen esta proteína, donde las secuencias 5'-GAG GTC ATC TTC AAA ACG GAT-3' y 5'-CTA CTA GAG TCT TAC CAC CTC -3' corresponden al oligonucleótido forward y reverso, respectivamente. Para ambos cebadores, todos los valores de ΔG en la formación de horquillas y autodímeros son mayores a -5 (no significativos), con un porcentaje de CG de 42.9 y 47.6%, y una diferencia de temperaturas de 1.8°C. La mejor temperatura es la del carril 3 (61.8°C). (Figura 5).
Expresión de las proteínas por E. coli BL21
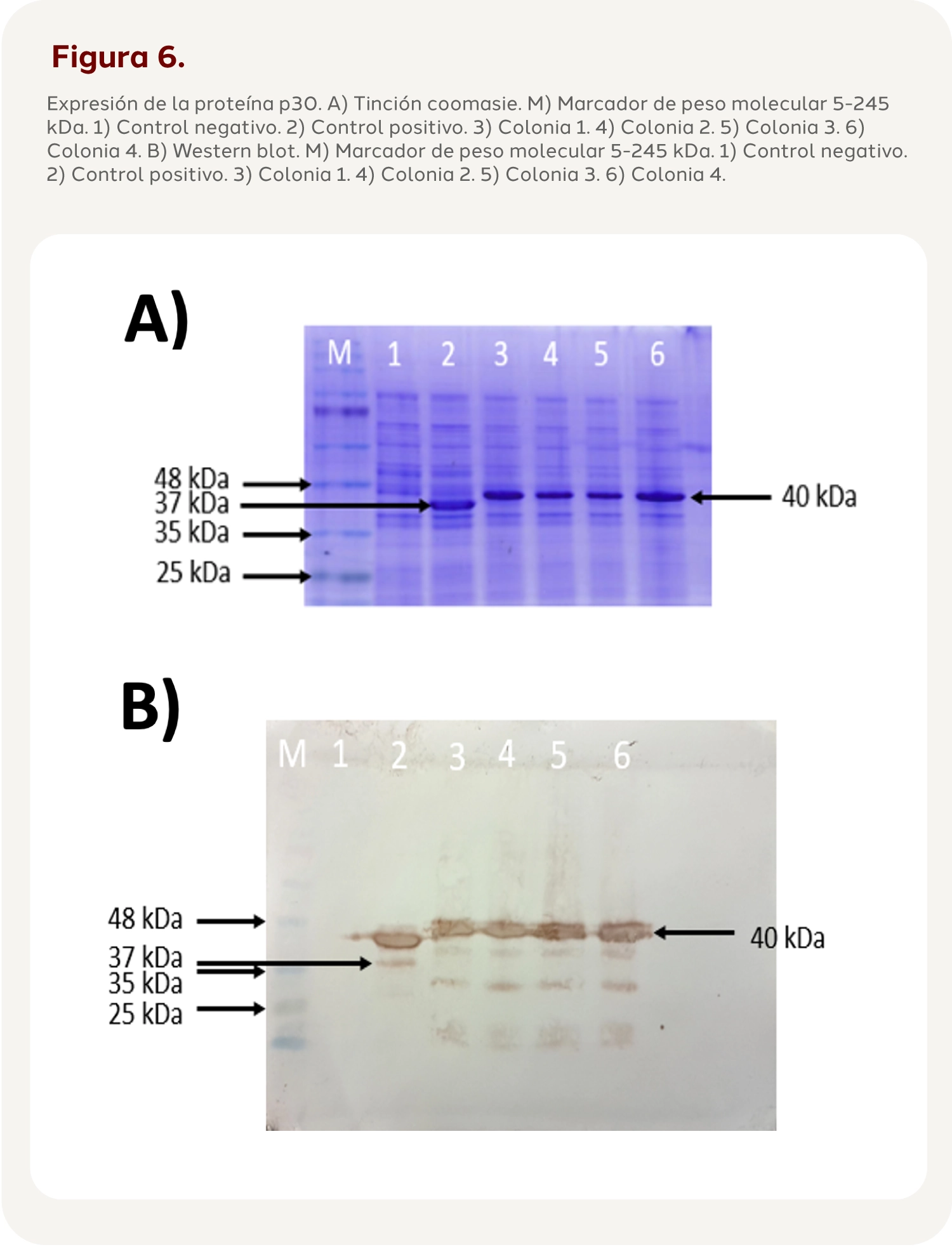
Se obtuvieron 4 colonias de E. coli expresoras de p30 que se indujeron con IPTG (isopropil β-D-1-tiogalactopiranósido). Para la detección y análisis de dichas proteínas una vez expresadas en el cultivo, se usan técnicas como la tinción coomassie y Western blot. Con la tinción coomassie se puede conocer, el peso molecular de la proteína de interés; en este caso, para la p30 es de 33 kDa y para la p72, de 42 kDa. (Figura 6 y 7)
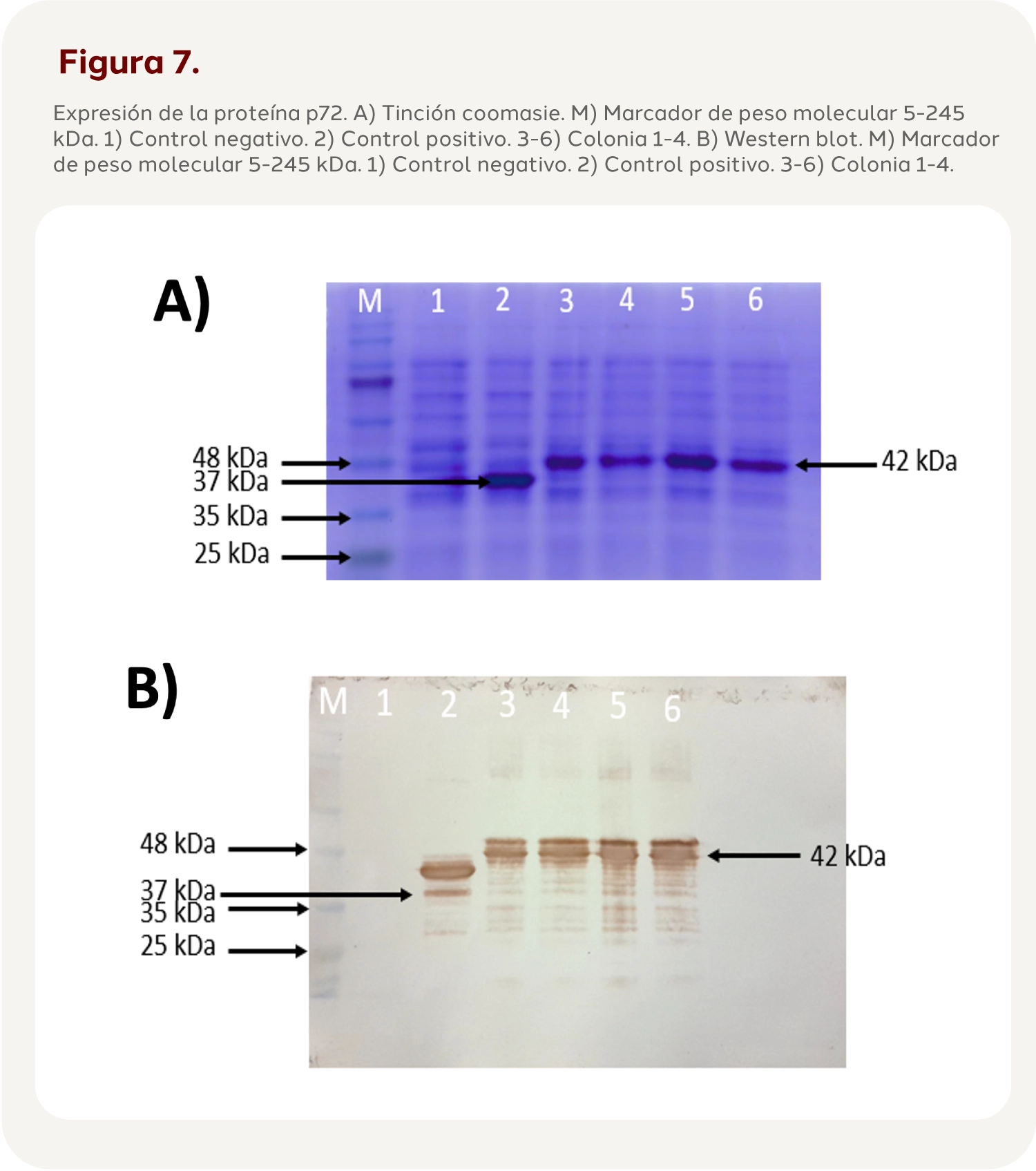
Purificación de las proteínas
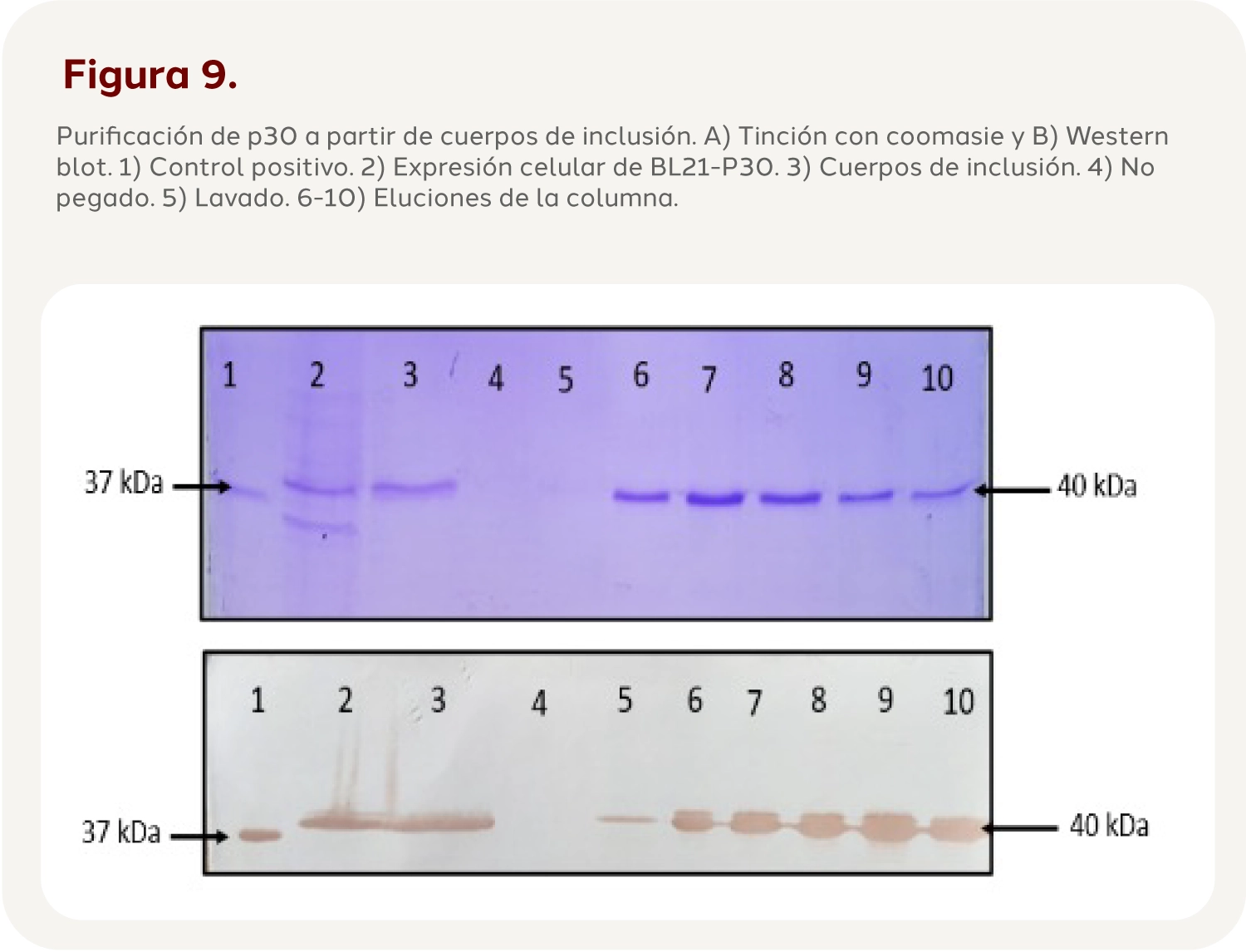
Como se puede observar en la figura anterior, la mayor parte de la proteína P72 se encuentra en forma de cuerpos de inclusión, que corresponde a la fase insoluble, por lo que es necesario llevar a cabo los procesos de solubilización para su purificación. Después de la purificación mediante cromatografía IMAC de los cuerpos de inclusión se analizó el proceso mediante SDS-PAGE y WB. donde se puede observar que se recuperó la proteína p72 y p30 en las eluciones en un solo paso de purificación y la ausencia de la misma en las muestras de no pegado y lavado indica que la proteína de interés está siendo purificada correctamente (Figura 8 y 9).
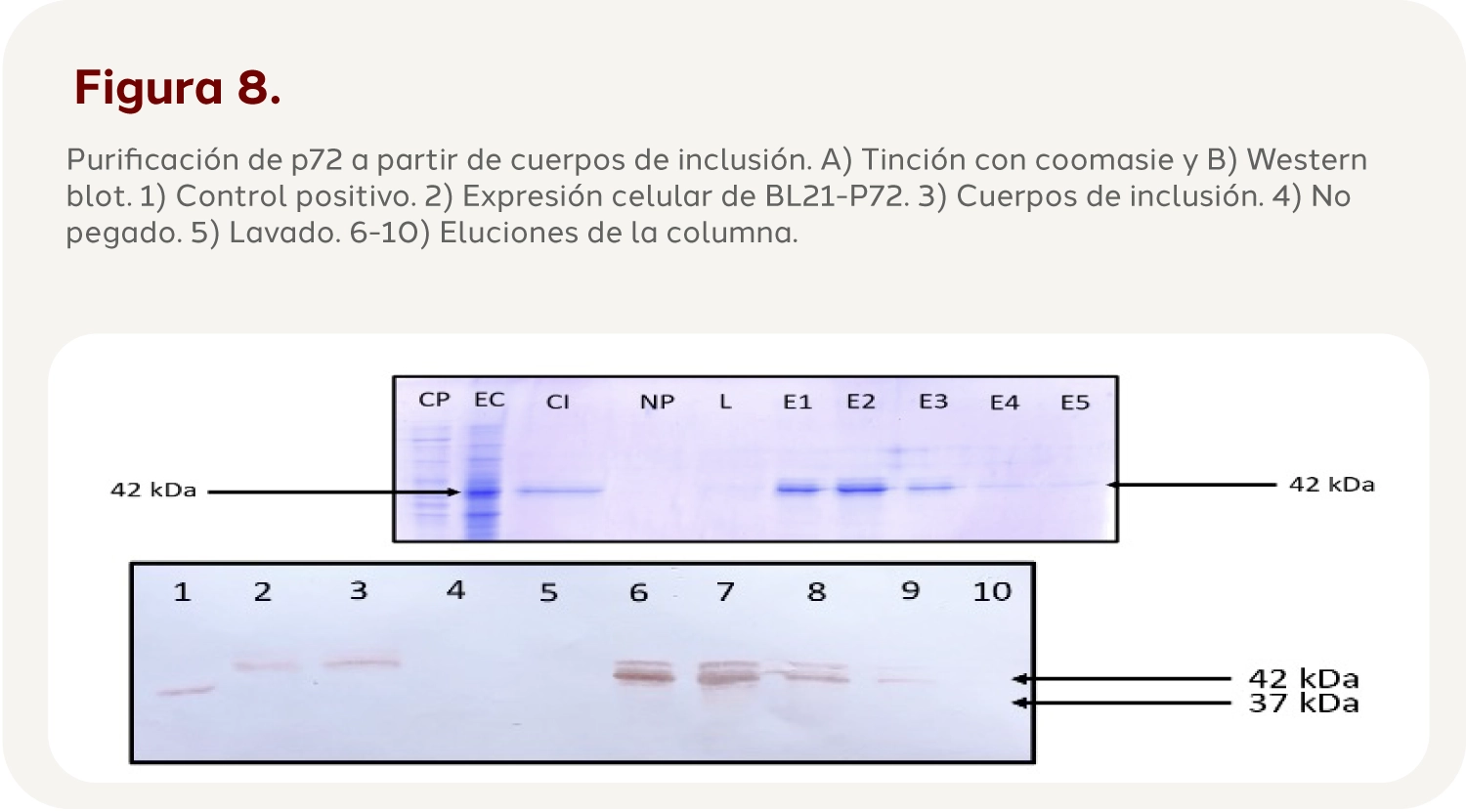
Cuantificación y rendimiento de p72 y p30
Las proteínas fueron dializadas para eliminar sales y se procedió a su cuantificación. Para la cuantificación de la concentración de proteína, se realizó la curva de calibración de Bradford usando una curva de BSA como estándar. La ecuación de la recta para la regresión fue y=0.013x+0.197 con R2=0.9719. La concentración de proteína p72 fue de 40.73 μg/mL, con un rendimiento de 230.807 μg/100 mL de cultivo. La concentración de proteína p30 fue de 30 μg/mL, con un rendimiento de 555 μg/100 mL de cultivo.
Conclusiones
En este trabajo se caracterizó de manera in silico la antigenicidad de la proteína p72 y p30 de la peste porcina africana para predecir los sitios antigénicos y seleccionar la región proteica apropiada para la expresión en E. coli y se logró generar un sistema de expresión recombinante derivado de dichas proteínas que pueda ser utilizado en un futuro como una herramienta de diagnóstico de la enfermedad. De esta forma se solidifica el primer desarrollo biotecnológico en México, basado en genes sintéticos de PPA, estudiados y producidos en colaboración con Canadá-USA y España para la atención de la enfermedad en caso de un brote en México, para el desarrollo de sistemas diagnósticos sensibles y específicos como medida preventiva para el país, que permita la identificación temprana y a gran escala de la PPA en laboratorios de nivel 2 de bioseguridad en México.
Agradecimientos y fuente financiera
El presente trabajo se llevó a cabo en el CENID-SAI, Laboratorio de Epizootiología, sede Palo Alto, Ciudad de México. Fue parcialmente financiado por el proyecto: “Proyectos de apoyo a la Investigación, PROCINORTE, No. SIGI: 1259436381”. Beca CONAHCYT CVU: 1139465.
Bibliografía
Ji. C., Jiang, J., Wei, Y., Wang, Z., Chen, Y., Mai, Z., Cai, M., Qin, C., Cai, Y., Yi, H., Liang, G., Lu, G., Gong, L., Zhang, G. and Wang, H. (2021). A Method for the Analysis of African Swine Fever by Viral Metagenomic Sequencing. Rev. Front. Vet. Sci. 8:766533. https://doi.org/10.3389/fvets.2021.766533
Sun, W., Zhang, H., Fan, W., He, L., Chen, T., Zhou, X., Qi, Y., Sun, L., Hu, R., Luo, T., Liu, W. and Li, J. (2021). Evaluation of Cellular Immunity with ASFV Infection by Sw Antigen (SLA)—Peptide Tetramers. Rev. Viruses; 13(11): 2264. https://doi.org/10.3390/v13112264
Wu, K., Zhang, Y., Zeng, S., Liu, X., Li, Y., Li, X., Chen, W., Li, Z., Qin, Y., Chen, J., Fan, S. (2022). Development and Application of RAA Nucleic Acid Test Strip Assay and Double RAA Gel Electrophoresis Detection Methods for ASFV and CSFV. Rev. Front Mol Biosci. Jan 31;8:811824. https://doi.org/10.3389/fmolb.2021.811824