Número:
- Vol. 3
- Num. 18
- Noviembre - Diciembre
Ganaderia.com
Autores:
 Yolanda Daniela
Yolanda Daniela Carrillo Huerta
Nacionalidad: Mexicana
Grado académico: Maestra en Producción Pecuaria
 A.J.
A.J. Gutiérrez Chávez
 J.J.
J.J. Guzmán Rodríguez
 P.D.
P.D. Loeza Lara
ISSN-e:
2992-7293
Capacidad lítica de un bacteriófago sobre escherichia coli multirresistentes aisladas de cuadros de mastitis en bovinos
Carrillo-Huerta YD.1, Guzmán-Rodríguez JJ.2, Loeza-Lara PD.3, Gutiérrez-Chávez AJ.1,4
1Programa de Maestría Interinstitucional en Producción Pecuaria, DICIVA, Universidad de Guanajuato, 2Instituto de Ciencia, Tecnología e Innovación del estado de Michoacán, 3Universidad de la Ciénega del estado de Michoacán de Ocampo, 4Departamento de Veterinaria y Zootecnia, DICIVA, Universidad de Guanajuato.
La mastitis bovina es el principal problema de la industria lechera, la cual afecta a la economía y sustentabilidad de las unidades de producción, y contribuye al aumento de riesgos para la salud pública debido a la presencia de patógenos resistentes a los antimicrobianos. Escherichia coli es el principal patógeno involucrado en la mastitis ambiental, con un número creciente de casos multirresistentes a los antibióticos (MRA) en los últimos años. El objetivo de este estudio fue evaluar la capacidad lítica de un bacteriófago E. coli multirresistentes aisladas de cuadros de mastitis en bovinos. Se obtuvieron 19 aislados MRA de E. coli, con índices de multirresistencia a los antibióticos (IMA) desde 0.36 a 1.00. El fago de E. coli mostró un 100% de capacidad para lisar los aislados utilizados en el presente estudio, resultados que implican una potencial alternativa para incorporarse como una herramienta en los protocolos de control de la mastitis bovina, particularmente en aquellos casos donde las bacterias muestran una nula respuesta a los antibióticos convencionales.
Palabras clave: multirresistencia, fagoterapia, mastitis ambiental.
Introducción
Para el 2050, está previsto que la demanda mundial de productos de origen animal incremente alrededor de un 38% (Komarek et al., 2021). Esto representa no solo un reto, sino una oportunidad de crecimiento para la producción de leche en México. El país ocupa el puesto décimo quinto a nivel mundial en producción de leche de bovino; sin embargo, todavía presenta un déficit de producción aproximada de 3 mil millones de litros que deben importarse de países como Estados Unidos de América (SIAP, 2022).
La mastitis es el problema más común dentro de las unidades de producción de leche de bovino, representando una enfermedad que afecta tanto la calidad como la cantidad de la leche, que genera un alto impacto al medio ambiente y a la sustentabilidad de la industria lechera (Puerto et al., 2021). Se han calculado las pérdidas asociadas a la mastitis en aproximadamente 2.8 litros por vaca afectada, lo cual, junto a los costos directos (pérdidas de leche, de animales, tratamientos) e indirectos (disminución de producción, reemplazos, problemas reproductivos) representan alrededor de MXN$8,880.00 por cada caso clínico (Rollin et al., 2015).
El principal tratamiento de la mastitis es la aplicación de antibióticos convencionales; sin embargo, los protocolos de prevención y control en la industria lechera están formulados para la mastitis contagiosa (siendo Staphylococcus aureus su principal patógeno), lo cual ha generado dos principales problemas en años recientes: que surjan más casos de mastitis ambiental (cuyo principal patógeno es Escherichia coli) y que dichos casos estén causados por bacterias multirresistentes a los antibióticos (Klaas & Zadoks, 2017; Xiangbin et al., 2020).
La Organización Mundial de la Salud (OMS, 2014) estima que, para el año 2050, el número de muertes atribuibles a la resistencia a los antibióticos será de 10 millones al año, con un costo aproximado de 100 trillones de dólares (Smith & Coast, 2013). Por este motivo, es de vital importancia encontrar estrategias alternativas a los antibióticos, especialmente para las bacterias clasificadas como prioritarias por la OMS (2024), entre las que se encuentra Escherichia coli, ya que representan un riesgo significativo para la salud pública, especialmente para los trabajadores de la industria pecuaria (Hao et al., 2024).
Además de la generación de resistencia antimicrobiana, los residuos de antibióticos representan otro de los mayores problemas para la salud pública. Una vez consumidos, estos residuos, encontrados en los productos pecuarios, generan reacciones tóxicas y alérgicas, que pueden incluir daños a largo plazo en su papel como agentes carcinógenos y teratógenos (Menkem et al., 2019).
En los últimos años, se han estudiado alternativas al uso de antibióticos convencionales, entre las que se encuentran los extractos de plantas, las nanopartículas de metal, las bacteriocinas y los bacteriófagos (Zaatout, 2022).
Los bacteriófagos (o fagos) son virus que infectan y lisan a las bacterias; son altamente específicos, ya que al infectar solamente a una especie o, incluso, a una cepa particular de bacteria, la lisis es provocada a las bacterias patógenas invasoras, y no a las células de los seres vivos (Murray et al., 2017).
La terapia de bacteriófagos (fagoterapia) resulta beneficiosa por varios factores, ya que no se ha demostrado que los fagos provoquen daño a los seres humanos, los animales ni al medio ambiente; son capaces de atravesar barreras naturales como la hematoencefálica, por lo que pueden alcanzar sitios localizados de infección dentro de los organismos vivos; además, los fagos tienen un sistema de autorregulación, ya que su replicación depende de la existencia de bacterias en el organismo (Kutter et al., 2020).
Con el objetivo de contribuir a la búsqueda de alternativas terapéuticas para la mastitis bovina, en el presente estudio se enfrentó un bacteriófago de Escherichia coli sobre aislados multirresistentes para registrar su eficacia lítica.
2. Materiales y métodos
2.1. Identificación morfológica y bioquímica de los aislados
Los aislados de E. coli del presente estudio fueron seleccionados del Banco Biológico de Materiales de la Universidad de la Ciénega del Estado de Michoacán de Ocampo, los cuales fueron obtenidos de vacas diagnosticadas con mastitis. Un total de 19 aislados fueron reactivados en el laboratorio de Anatomía y Patología de la Universidad de Guanajuato. 100 μL de cada muestra fue extendida homogéneamente sobre las superficies de agar MacConkey y agar Eosina y Azul de metileno en cajas Petri; posteriormente, las cajas se dejaron secar dentro de una campana de bioseguridad y se incubaron a una temperatura de 36 ± 1°C. Las cajas se leyeron después de 24-48 h, tal como está descrito en el Consejo Nacional de Mastitis (NMC, 1999), para identificar el crecimiento de colonias sugerentes a E. coli. Los aislados fueron identificados morfológica y bioquímicamente, incluyendo las pruebas de indol, citrato, motilidad, producción de ácido sulfhídrico (H2S), producción de gas, fermentación de carbohidratos (lactosa, glucosa y sacarosa), e hidrólisis de urea (Sykes & Rankin, 2014). Todos los aislados se cultivaron en caldo Luria Bertani (LB) a 36 ± 1°C, y resguardados a -20°C con 15% de glicerol.
2.2. Determinación de la eficacia lítica del fago de Escherichia coli
El fago de E. coli fue aislado, purificado y provisto por la compañía SEDEBIO®. Se determinó la capacidad lítica del fago a través de la prueba de la gota, con modificaciones (Poxleitner et al., 2018). 1 mL de cada solución se extendió de manera homogénea utilizando hisopos estériles de algodón sobre placas Petri con agar LB dividido en cuatro cuadrantes. Después, una gota de 20 μL de la solución de fagos, a una concentración de 4.8X105, se colocó sobre tres de los cuadrantes de cada caja inoculada con E. coli, colocando en los cuadrantes número 4 una gota de agar LB estéril como control negativo. Las cajas se secaron y se incubaron a 36 ± 1°C durante 18 a 24 h para su posterior lectura y observación de la actividad lítica del fago, el cual fue determinado por la presencia o ausencia de zonas claras (calvas) en la superficie del agar. Los diámetros de las zonas de lisis fueron medidos y registrados en mm.
3. Resultados
El bacteriófago de Escherichia coli tuvo una efectividad del 100% de lisis sobre los 19 aislados de leche de vacas diagnosticadas con mastitis, con un diámetro de calvas promedio de 2.26 mm (Cuadro 1).
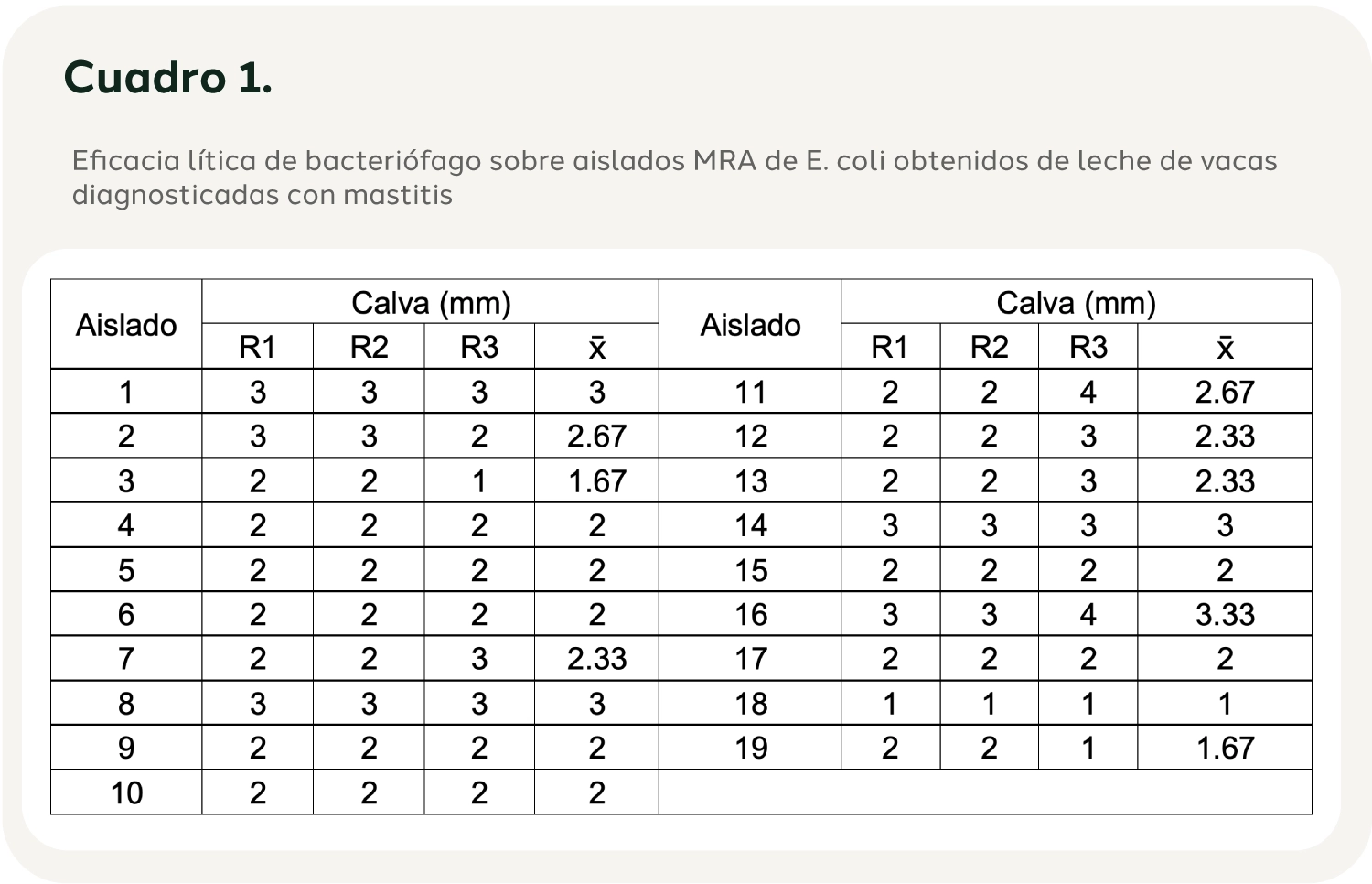
4. Discusión
Los patógenos ambientales y contagiosos causantes de mastitis en las unidades de producción de leche de bovino, pero sobre todo E. coli, requieren estrategias alternativas que mitiguen la resistencia antimicrobiana que ha ido en aumento en los últimos años. Dentro de estas estrategias, los bacteriófagos y la fagoterapia pueden considerarse una alternativa prometedora ya que, además de igualar o mejorar los efectos terapéuticos de los antibióticos convencionales, contribuyen a la preservación de la salud pública y del medio ambiente (Carrillo-Huerta, 2024).
Los resultados del presente estudio han resultado significativamente superiores en comparación con lo descrito por otros autores, como el de Abdulhussein & Abdulsattar (2022), quienes aislaron dos bacteriófagos de E. coli (AAA1 y AAA2) en Iraq, y registraron una eficacia lítica de solo un 12 y 3%, respectivamente. Mientras que Sahin et al. (2022), probaron tres fagos y obtuvieron porcentajes de lisis del 25, 64.5 y 79.2%, respectivamente, sobre sus aislados de E. coli. Otro fago de Escherichia coli fue aislado y probado por Xiao et al. (2023), el cual mostró eficacia lítica sobre 21 de sus 92 aislados (22.8%); resultados similares fueron encontrados por Elbahnasawy & El Sayed (2021), en donde se probaron otros tres fagos y se obtuvieron porcentajes de eficacia lítica de 39.1, 28.9 y 32.3% respectivamente, sobre aislados de E. coli, de los cuales, el 60% estuvieron clasificados como MRA. Dos fagos de E. coli fueron enfrentados a 24 aislados de E. coli en un estudio llevado a cabo por Fu et al. (2021), donde se registró una eficacia lítica del primer fago sobre la mitad de los aislados (7 de ellos MRA), y del segundo fago sobre 10 de los aislados (todos ellos MRA). Al compararse los patrones de resistencia a los antibióticos con la actividad lítica observada en los estudios antes mencionados, se demostró que no hubo asociación entre ambas variables, situación que se confirma con los resultados del presente estudio, al haberse obtenido un 100% de eficacia lítica sobre 19 aislados de E. coli multirresistentes.
5. Conclusión
De los 19 aislados de E. coli multirresistentes seleccionados para este estudio, presentaron un índice de multirresistencia a los antibióticos de 0.36 a 1.00, considerando que un valor igual o mayor a 0.2 es de importancia sanitaria. El bacteriófago de Escherichia coli demostró un 100% de capacidad lítica en contra de los aislados obtenidos de leche de vacas infectadas con mastitis utilizados en el presente estudio, lo cual vuelve al fago un prospecto prometedor para ser utilizado como un agente terapéutico en contra no solo de la mastitis ambiental ocasionada por Escherichia coli, sino contra cualquier cuadro ocasionado por dicha bacteria en animales e, incluso, en seres humanos.
6. Agradecimientos
Los autores agradecen a Servicios y Desarrollo de Biofármacos S, A. (SEDEBIO™) y a la DAIP-Universidad de Guanajuato por el proyecto CIIC-012-2024.
7. Referencias
Abdulhussein, A. A., Abdulsattar, B. O. 2022. Isolation and characterization of two novel phages as a possible therapeutic alternative against multi-drug resistant E. coli. Gene Reports. 28: 1-9 https://doi.org/10.1016/j.genrep.2022.101644
Carrillo-Huerta, Y.D., 2024. Capacidad lítica in vitro de bacteriófago contra Escherichia coli aislada de bovinos. Tesis de Maestría. Programa de Maestría en Producción Pecuaria. División de Ciencias de la Vida, Universidad de Ganajuato. México.
Elbahnasawy, M. A., El Sayed, E. E., Azzam, M. I., 2021. Newly isolated coliphages for bio-controlling multidrug-resistant Escherichia coli strains. Environmental Nanotechnology, Monitoring & Management. 16: 1-12 https://doi.org/10.1016/j.enmm.2021.100542
Fu, P., Zhao, Q., Shi, L., Xiong, Q., Ren, Z., Xu, H., Chai, S., Xu, Q., Sun, X., Sang, M., 2021. Identification and characterization of two bacteriophages with lytic activity against multidrug-resistant Escherichia coli. Virus Research. 291: 198196 https://doi.org/10.1016/j.virusres.2020.198196
Hao, R., Shoaib, M., Tang, M., Cao, Z., Liu, G., Zhang, Y., Wang, S., Shang, R., Zhang, H., Pu, W., 2024. Genomic insights into resistome, virulome, and mobilome as organic contaminants of ESKAPE pathogens and E. coli recovered from milk, farm workers, and environmental settings in Hainan, China. Emerging Contaminants. 10: 100385 doi: 10.1016/j.emcon.2024.100385
Klaas, I. C., Zadoks, R. N., 2017. An update on environmental mastitis: Challenging perceptions. Transboundary and Emerging Diseases. 65: 166-185 https://doi.org/10.1111/tbed.12704
Komarek, A. M., Dunston, S., Enahoro, S., Godfray, H. C. J., Herrero, M., Mason-D’Croz, D., Rich, K. M., Scarborough, P., Springmann, M., Sulser, T. B., Wiebe, K., Willenbockel, D. 2021. Income, consumer preferences, and the future of livestock-derived food demand. Global Environmental Change. 70: 1-11 https://doi.org/10.1016/j.gloenvcha.2021.102343
Kutter, E., Hoyle, N., Eisner, W., Kuhl, S., Alavidze, Z., Blasdel, B. G., 2020. Phage therapy: Bacteriophages as natural, self-limiting antibiotics. En Pizzorno, J. E., Murray, M. T., (Eds.), Textbook of Natural Medicine (pp. 777-787). Churchill Livingstone. http://dx.doi.org/10.13140/2.1.1100.3840
Menkem, Z. E., Ngangom, B. L., Tamunjoh, S. S. A., Boyom, F. F. 2019. Antibiotic residues in food animals: Public health concern. Acta Ecologica Sinica 39(5): 412-415 https://doi.org/10.1016/j.chnaes.2018.10.004
Murray et al., 2017). Murray, P. R., Rosenthal, K. S., Pfaller, M. A., 2017. Microbiología médica (9° ed.). Elsevier Health Sciences. https://books.google.com.mx/books?hl=es&lr=&id=GOaVDgAAQBAJ&oi=fnd&pg=PP1&dq=.+Microbiolog%C3%ADa+m%C3%A9dica+(9%C2%B0+ed.).+Elsevier+Health+Sciences.&ots=hSi_IGNVno&sig=3TuMxlPqj0Lc9G8kmwtfTHTiFPs#v=onepage&q=.%20Microbiolog%C3%ADa%20m%C3%A9dica%20(9%C2%B0%20ed.).%20Elsevier%20Health%20Sciences.&f=false
NMC, 1999. National Mastitis Council. Laboratory handbook on bovine mastitis, tercera edición. New Prague, Minnesota. Disponible en https://www.academia.edu/50651208/Laboratory_Handbook_on_Bovine_Mastitis
OMS, 2014. Organización Mundial de la Salud. Antimicrobial resistance: global report on surveillance. Disponible en: https://apps.who.int/iris/handle/10665/112642 Consultado el 16 de noviembre del 2022
OMS, 2024. Organización Mundial de la Salud. WHO bacterial priority pathogens list, 2024: Bacterial pathogens of public health importance to guide research, development and strategies to prevent and control antimicrobial resistance. Disponible en: https://who.int/publications/i/item/9789240093461 Consultado el 30 de julio del 2024
Poxleitner, M., Pope, W., Jacobs-Sera, D., Sivanathan, V., Hatfull, G., 2018. Phage Discovery Guide. Howard Hughes Medical Institute https://seaphagesphagediscove Consultado el 20 de mayo de 2023
Puerto, M. A., Shepley, E., Cue, R. I., Warner, D., Dubuc, J., Vasseur, E., 2021. The hidden cost of disease: I. Impact of the first incidence of mastitis on production and economic indicators of primiparous dairy cows. Journal of Dairy Science. 104: 7932-7943 https://doi.org/10.3168/jds.2020-19584
Rollin, E., Dhuyvetter, K.C., Overton, M. W., 2015. The cost of clinical mastitis in the first 30 days of lactation: An economic modeling tool. Preventive Veterinary Medicine. 122: 257-264 https://doi.org/10.1016/j.prevetmed.2015.11.006
Sahin, K., Bao, H., Zhu, S., Soleimanbi-Delfan, A., He, T., Mansoorianfar, M., Wang, R., 2022. Biocontrol of O157:H7, and colistin-resistant MCR-1-positive Escherichia coli using a new designed broad host range phage cocktail. LWT. 254: 1-11 https://doi.org/10.1016/j.lwt.2021.112836
SIAP, 2022. Servicio de Información Agroalimentaria y Pesquera. Escenario mensual de productos agroalimentarios. Disponible en: https://nube.siap.gob.mx/poblacion_ganadera/ Consultado el 01 de agosto de 2024
Smith, R., Coast, J., 2013. The true cost of antimicrobial resistance. BMJ. 346: 1-5 https://doi.org/10.1136/bmj.f1493
Sykes, J. E., Rankin, S. C., 2014. Isolation and identification of aerobic and anaerobic bacteria. En Sykes, J. E. (Ed.), Canine and Feline Infectious Diseases. Pp. 17-28. Saunders http://dx.doi.org/10.1016/B978-1-4377-0795-3.00003-
Xiangbin, S., Huang, X., Xu, H., Zhang, C., Chen, S., Liu, F., Guan, S., Zhang, S., Zhu, K., 2020. The prevalence of pathogens causing bovine mastitis and their associated risk factors in 15 large dairy farms in China: An observational study. Veterinary Microbiology. 247: 1-7 https://doi.org/10.1016/j.vetmic.2020.108757
Xiao, T., Zhu, X., Wang, W., Jia, X., Guo, C., Wang, X., Hao, Z., 2023. A novel lytic bacteriophage against colistin-resistant Escherichia coli isolated from different animals. Virus Research. 329: 1-9 https://doi.org/10.1016/j.virusres.2023.199090
Zaatout, N., 2022. An overview on the mastitis-associated Escherichia coli: Pathogenicity, host immunity and the use of alternative therapies. Microbiological Research. 256: 1-14 https://doi.org/10.1016/j.micres.2021.126960