Número:
- Vol. 3
- Num. 17
- Septiembre - Octubre
Avicultura.mx
Autores:
 Elkin Giovanny
Elkin Giovanny Quiroga Calderon
Nacionalidad: Colombiano
Grado académico: Maestro en Ciencia Animal
ISSN-e:
2992-7293
Monitoreo del agua, suelo y excremento para la identificación de parásitos gastrointestinales en gallinas ponedoras
RESUMEN
En la avicultura durante todo el ciclo productivo de las gallinas suele presentarse infecciones de tipo parasitario gastrointestinal, generando síntomas de malestar, pérdida de peso en los animales, anemias y diarreas. El estudio se realizó en el corral de gallinas ponedoras del Rancho Universitario de la Universidad Autónoma de Ciudad Juárez (RU-UACJ), ubicado en el Valle de Juárez, municipio de Práxedis Guerrero, Chihuahua, con el objetivo de monitorear el agua, suelo y excremento de gallinas de postura del RU-UACJ para de identificar parásitos gastrointestinales los cuales sirven como indicadores para prevenir futuros contagios parasitario. Durante el desarrollo del estudio se recolectaron muestras de agua, suelo y excremento de las gallinas en las estaciones de otoño del 2020 e invierno 2020-2021, a las cuales se les realizó sus respectivos análisis para la identificación de parásitos gastrointestinales en el Laboratorio de la División Multidisciplinaria de Nuevo Casas Grandes de la Universidad Autónoma de Ciudad Juárez. De acuerdo a los análisis de laboratorio se identificaron en total cuatro géneros de parásitos gastrointestinales de la clase de helmintos nematodos; en el agua se detectó Toxocara y Ancylostoma, en el suelo Strongyloides, Ascaris, Toxocara, y Ancylostoma, mientras que para las muestras de excremento se identificó Ascaris. Un monitoreo del agua, suelo y excremento de los animales ayuda a identificar la presencia o ausencia de microorganismos patógenos y en base a ello poder aplicar las Buenas Prácticas Ganaderas.
Palabras claves: agua; avicultura; excremento; suelo; parásitos.
INTRODUCCIÓN
En toda explotación pecuaria es primordial mantener un estado óptimo de salud y bienestar animal a través del empleo de las buenas prácticas ganaderas (OIE, 2019), inclusive la Ley Federal de Sanidad Animal en México, resalta su aplicabilidad mencionando que estas ayudan a reducir problemas sanitarios en los animales.
En toda actividad pecuaria durante su desarrollo pueden llegar a existir diversos factores de riesgo generando enfermedades infecciosas asociadas al entorno y al manejo animal, las cuales llegan a afectar el estado sanitario de los animales; por esta razón es importante conocer su comportamiento y condiciones de alojamiento (Ratanapob et al., 2012; Barasona et al., 2014).
En el arte de la avicultura durante el desarrollo productivo de las gallinas suele presentarse infecciones de tipo endoparasitario, generado por agentes patógenos como los de clase helmintos y protozoos (Camposano, 2018). Es por ello que frente a un cuadro de infección parasitaria gastrointestinal, estos parásitos predisponen a las aves a tener mermas significativas de peso corporal, anemia y diarreas (Ensucho et al., 2015).
Es de resaltar que uno de los mecanismos de propagación parasitaria gastrointestinal se atribuye al contacto de agua y suelo contaminado (Keraita y Amoah, 2011); ya que en algunas ocasiones en los suelos se albergan huevos o larvas de parásitos, además de utilizar el agua como medio de incubación (Ojha et al., 2104; Milano et al., 2007). También se ha demostrado que una ingesta de agua contaminada tiende a disminuir la producción de huevo en las gallinas (Rueda, 2020).
Por lo anterior, el objetivo de este estudio fue monitorear el agua, suelo y excremento de gallinas de postura del Rancho Universitario de la Universidad Autónoma de Ciudad Juárez para de identificar parásitos gastrointestinales los cuales sirven como indicadores para prevenir futuros contagios parasitario.
MATERIALES Y MÉTODOS
El presente estudio estuvo bajo la dirección de la Ph. D. Zarhelia Carlo Rojas y la Codirección de la Ph. D. Ana Bertha Gatica Colima, vinculadas al Instituto de Ciencias Biomédicas, Programa de Maestría en Ciencia Animal de la Universidad Autónoma de Ciudad Juárez.
El estudio se realizó en el corral de gallinas ponedoras del RU-UACJ, ubicado en el Valle de Juárez, municipio de Práxedis Guerrero, Chihuahua, con una altitud de 1090 msnm y coordenadas geográficas de referencia 31° 21' 20" N y 105° 59' 59" O. La zona se tiene un clima árido extremoso, con una temperatura máxima de 43ºC y mínima de -10ºC; con una temperatura promedio anual es de 16ºC, la precipitación pluvial media anual es de 275 milímetros, y con vientos dominantes del Suroeste (INEGI, 2020).
Para el desarrollo del estudio se recolectaron muestras de agua, suelo y excremento de las gallinas en las estaciones de otoño del 2020 e invierno 2020-2021, a las cuales se les realizó sus respectivos análisis para la identificación de parásitos gastrointestinales en el Laboratorio de la División Multidisciplinaria de Nuevo Casas Grandes de la Universidad Autónoma de Ciudad Juárez. Es de resaltar que las zonas agrícolas del (RU-UACJ) se riegan con agua proveniente del canal del rio Bravo y el piso del corral de las gallinas es en tierra. También se determinó el porcentaje de prevalencia parasitaria mediante la fórmula: P= (n/N) x100 (OPS, 2018).
Dónde:
P = prevalencia
n = número de animales positivos
N = total de animales.
En relación a las muestras de agua, su colecta se obtuvo del canal de riego y otra de la llave de agua potable, acorde a la Norma Oficial Mexicana NOM-230-SSA1-2002 y Norma Mexicana NMX-AA-003-1980. Para ello se utilizó garrafones de plástico de 6 litros, los cuales se desinfectaron previamente con hipoclorito de sodio al 10 % y lavados con agua potable, posteriormente se enjuagó con agua destilada. El análisis de las muestras se realizó de acuerdo protocolo establecido por Maya (2017), protocolo adaptado de la norma oficial mexicana NMX-AA-113-SCFI-2012 para la detección de huevos de helminto.
La recolecta de las muestras del suelo se realizó a lo establecido en la Norma Mexicana NMX- AA-132-SCFI-2016, utilizando bolsas de polietileno para el almacenamiento y etiquetado de las muestras, para ello se recolectó 500 gramos de suelo por muestra a una profundidad de 0 a 5 cm a partir de la superficie. Las muestras se obtuvieron del corral de las gallinas, adicionalmente también se tomaron muestras en las áreas agrícolas aledañas del corral, posteriormente las muestras se transportaron refrigeradas al laboratorio para su respectivo análisis y detección de parásitos gastrointestinales mediante la técnica de flotación Sheather (Polo 2006).
En cuanto a las muestras de excremento, se realizó la toma de una muestra compuesta de excretas por estación de año, recolectada durante tres días consecutivos. Las muestras se tomaron directamente del piso del corral después de defecación espontánea, manteniéndolas en una nevera a 4ºC (PANAFTOSA 2017). Posteriormente se realizaron análisis coproparasitoscópicos de Faust y sedimentación (Figueroa-Castillo et al., 2015) y McMaster (OPS, 2020).
RESULTADOS Y DISCUSIÓN
De acuerdo a los análisis de laboratorio se identificaron en total cuatro géneros de parásitos gastrointestinales de la clase de helmintos nematodos; en el agua se detectó Toxocara y Ancylostoma (tabla 1); en el suelo Strongyloides, Ascaris, Toxocara, y Ancylostoma (tabla 2); mientras que para las muestras de excremento Ascaris (tabla3).

En las muestras de llave de agua potable no se detectó presencia de huevos de helmintos. No obstante las muestras del canal de riego fueron positivas, siendo estas un riesgo para la salud ya que supera el límite máximo permisible según la norma oficial mexicana NMX-AA-113-SCFI-2012.
En cuanto a los huevos de parásitos de helmintos obtenidos en las muestras de agua de este estudio, se coincide con Maya (2017), quien reportó la presencia de Toxocara en una evaluación de riesgo con agua tratada, residual y de uso agrícola en Nuevo Casas Grandes, Chihuahua. Por lo general este helminto se halla con mayor frecuencia en agua (OMS 2004), y en efecto ante este hallazgo se considera como una señal de alerta el agua del canal de riego del río Bravo, ya que no se recomienda utilizarla como fuente de hidratación en el RU-UACJ porque puede fungir como un vector parasitario.
Por otro lado no se concuerda con los géneros de parásitos detectados por Olivas et al., (2013), quienes reportaron ooquistes de Cryptosporidium y Giardia en el agua en el Valle de Juárez representando el 92.3% de 14 localidades estudiadas, considerando también que el agua proveniente del canal de riego no es segura como bebida.
El hallazgo de los helmintos en el agua del presente estudio puede estar asociado a que el agua del canal de riego se encontraba con abundante presencia de distintos materiales particulado y de lodos, además de ser una fuente de hidratación para animales silvestres, de producción y perros domésticos, los cuales en algunas ocasiones suelen defecar de forma instintiva en las orillas del canal, y sus heces son arrastradas por la corriente hídrica, además también se constató que los bebederos del corral se encontraban a veces sucios porque las gallinas pisan el agua. En base a estas razones el agua del canal de riego se considera un riesgo sanitario para las gallinas exponiéndolas a un contagio de microorganismo patógenos y mortalidad de las aves, ya que algunas ocasiones se encontraron a las gallinas fuera de su corral hidratándose en las orillas del canal de riego y sus patas pueden ser un vehículo de transmisión parasitaria. En este sentido se concuerda con Rueda (2020), quien encontró en su estudio que las aves que se abastecen de agua sucia tienden a ser susceptibles a presentar síntomas de malestar y reducción de producción de huevo.
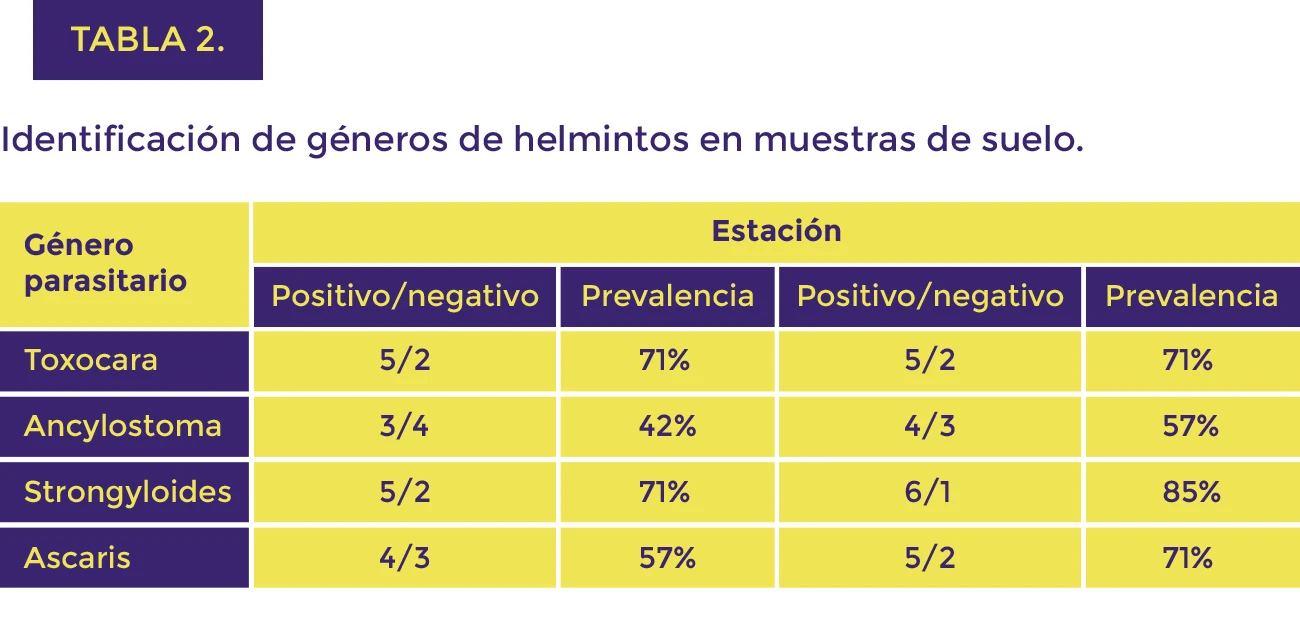
En cuanto a las muestras del suelo que fueron positivas en la identificación de géneros parasitarios se les determinó sus porcentajes de prevalencia, obteniendo que Toxocara presenta una prevalencia general de 71.4%, Ancylostoma 50%, Strongyloides 78.5% y Ascaris 64.2%.
El hallazgo de estos helmintos puede estar atribuido a que el suelo del RU-UACJ normalmente es regado con agua proveniente del canal principal del río Bravo que circula a lo largo del Valle de Juárez, por tal razón este podría contener y arrastrar huevos de helmintos y ooquistes de protozoos, además de que en las zonas agrícolas transita ganado vacuno, ovinos, caprinos, perros domésticos y fauna silvestre donde algunas veces estas especies animales suelen desechar sus heces directamente al suelo, las cuales pueden estar cargadas de huevos u ooquistes de parásitos contaminando el suelo con estos patógenos. Dentro de este contexto se concuerda con la OIE (2015), que menciona que en lugares concurridos por distintas especies de animales, será un entorno adecuado a la exposición, propagación y contagio de enfermedades.
Estas razones coinciden con los argumentos de Garza et al., (2001), quienes argumentan que una posible vía de contaminación parasitaria de los suelos en la zona del Valle de Juárez es atribuido al canal de riego, porque aparte de llevar aguas crudas, arrastra sólidos disueltos y estos lodos pueden estar cargados de microorganismos patógenos. Así mismo Flores et al., (2010), en su estudio señalan que la carga parasitaria detectada en el suelo de algunas zonas del Valle de Juárez se debe a que los suelos son regados con agua con agua residuales, las cuales pueden estar cargadas con microorganismos que contiene la materia fecal, sin embargo en su estudio reportaron la presencia de ooquistes de protozoos: Cryptosporidium parvum de 22 a 74 y de Giardia lamblia de 7 a 33 ooquistes. Estos parásitos difieren en absoluto con los obtenidos del presente estudio, razón por la cual las técnicas utilizadas no permitieron la detección de protozoos.
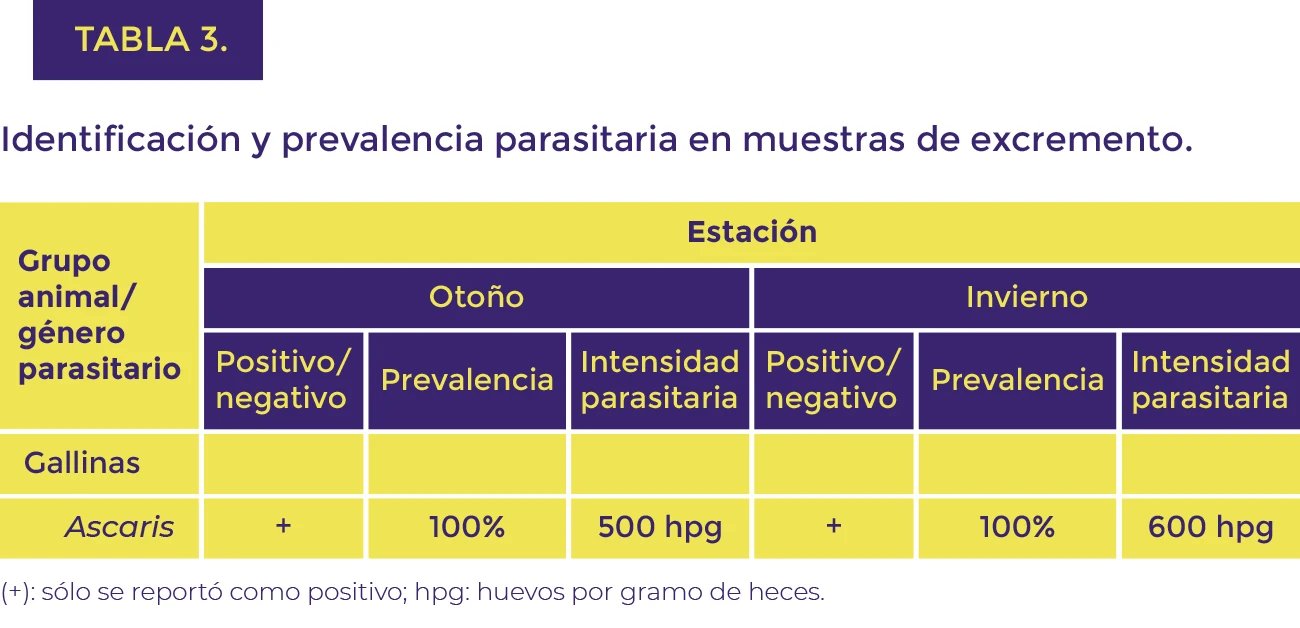
Con respecto a las muestras compuestas de excremento de las gallinas en el presente estudio, se identificó el género parasitario Ascaris con una prevalencia del 100%, este hallazgo se puede atribuir a que las gallinas algunas veces se fugan de su corral y frecuentan distintas áreas del RU-UACJ donde interactúan con otras especies de animales, por lo tanto, esto hace que las gallinas queden predispuestas a un contagio parasitario, además el piso del corral de las gallinas es en tierra y este elemento puede favorecer a una transmisión de patógenos en las gallinas, porque estas suelen escarbar y picotear el suelo constantemente en busca de lombrices donde de forma accidental pueden ingerir huevos de parásitos contenidos en el suelo. También se considera que la presencia de este parásito puede estar referido a la ausencia de un plan de control sanitario.
Dentro de este contexto se concuerda con lo señalado por Guerrero y Vásquez (2018) quienes reportan que gallinas criadas en piso de tierra presentan un alto riesgo de infección de Ascaris. Así mismo Olmo et al., (2015), en su estudio demostraron que las gallinas que son alojadas en corrales con piso de tierra son susceptibles a una infección parasitaria por Ascaris, mientras las que son albergadas en piso de cemento presentan un menor contagio de parásitos gastrointestinales. Del mismo modo Rodríguez (2004), menciona que las aves por instinto buscan comer lombrices, las cuales son huéspedes intermedios de Ascaris, además en el suelo se llega a encontrar huevos en etapa de larva infectiva.
CONCLUSIONES
Un monitoreo del agua, suelo y excremento de los animales ayuda a identificar la presencia o ausencia de microorganismos patógenos.
Los géneros parasitarios (Toxocara, Ancylostoma, Strongyloides y Ascaris) identificados en este estudio, sirven como indicadores para prevenir un futuro contagio parasitario y en base a ello poder aplicar las Buenas Practicas Ganaderas.
El agua del canal de riego del río Bravo se evidenció una alta presencia de huevos de parásitos (Toxocara con 10 y Ancylostoma con 1 en 5 litros de agua) por lo que no es recomendable como fuente de hidratación, ya que el superó el límite máximo permisible según la norma oficial mexicana NMX-AA-113-SCFI-2012.
En las muestras de suelo se detectaron cuatro géneros de parásitos y sus respectivas prevalencias generales (Toxocara 71.4%, Ancylostoma 50%, Strongyloides 78.5% y Ascaris 64.2%), la existencia de estos parásitos es porque los suelos son concurridos por diversas especies animales, además de ser irrigado con agua proveniente del canal de riego del río Bravo.
Con respecto a las muestras compuestas de excremento de las gallinas en el presente estudio, se identificó el género parasitario Ascaris con una prevalencia del 100% lo que indica que se requiere una desparasitación de las gallinas.
REFERENCIAS
Barasona, J.A., Latham, M.C., Acevedo, P., Armenteros, J.A., Latham, A.D., Gortázar, C. 2014. Spatiotemporal interactions between wild boar and cattle: Implications for cross-species disease transmission. Vet Res. 45:1-122
Camposano, P. 2018. Prevalencia de parásitos gastrointestinales en aves criollas. Tesis de Licenciatura. Universidad Politécnica Salesiana. Cuenca, Ecuador.
Flores, J. P., Ramírez, A., Olivas, E., Corral, B., Hurtado, R., Lizárraga, G., Salazar, A., Rodríguez, M., Agüero, L., Borrego, A., Gardea, J. 2010. Gastrointestinal diseases and causal effects in the Valle de Juárez, Chihuahua, México. Universidad Autónoma de Ciudad Juárez, (Colección Textos Universitarios, serie Investigación), 128 p. Vol. 5.
Ensucho, C., Herrera, Y., Montalvo, A., Almanza, M., Vergara, J., Pardo, E., y Gomez, L. (2015). Frecuencia de parásitos gastrointestinales en gallinas criollas (Gallus domesticus) en el departamento de Córdoba, Colombia. Redvet, 16(6), 1-10.
Figueroa-Castillo, J. A., Jasso Villazul, C., Liébano Hernández, E., Martínez Labat, P., Rodríguez Vivas, R. I., Zárate-Ramos, J. J. 2015. Técnicas para el diagnóstico de parásitos con importancia en salud pública y veterinaria. Cap. 3: Examen coproparasitoscópico. AMPAVE-CONASA. México, DF págs. 78-128.
Garza, V., Fernández, I., Flores, M. B., Hauad, L., Villarreal, L. 2001. Evaluación de riesgo a la salud en la comunidad de Loma Blanca (distrito de riego 009) Valle de Juárez (México), por exposición a aguas residuales no tratadas. RESPYN. Vol. 2, No 3.
Guerrero, D., Vásquez, O. 2018. Prevalencia de ascaridiosis (Ascaridia galli) en aves ponedoras, granja avícola Hannón, municipio de Nindirí, departamento de Masaya, septiembre-noviembre 2018. Tesis de licenciatura. Universidad Nacional Agraria. Managua, Nicaragua.
INEGI (Instituto Nacional de Estadística y Geografía) 2020. Disponible en: https://www.inegi.org.mx/
Keraita, B., Amoah, P. 2011. Fecal exposure pathways in Accra: a literature review with specific focus on IWMI?s work on wastewater irrigated agriculture. Report submitted to the Centre for Global Safe Water, Emory University, Atlanta, USA. Accra, Ghana: International Water Management Institute (IWMI). 43p.
Ley Federal de Sanidad Animal en México. Diario Oficial de la Federación. 7 de junio de 2012.
Maya, P. 2017. Detección de huevos de helmintos en agua tratada, residual y de uso agrícola y evaluación de riesgo por género en Nuevo Casas Grandes, Chihuahua. Tesis Maestría en Ciencias de la Salud Pública. Universidad Autónoma de Ciudad Juárez. Ciudad Juárez, México.
Milano, A.M., Oscherov, E.B., Legal, A.S., Espinoza, M.C. 2007. La vivienda urbana como ambiente de transmisión de algunas helmintiasis caninas de importancia zoonótica en el nordeste Argentino. Boletín de malariología y salud ambiental. 2007 diciembre; XLVII (2):199-204
Norma Mexicana NMX-AA-003-1980 Manejo y muestreo de aguas residuales. Diario Oficial de la Federación. 25 de marzo de 1980.
Norma Oficial Mexicana NOM-230-SSA1-2002, Salud ambiental. Agua para uso y consumo humano, requisitos sanitarios que se deben cumplir en los sistemas de abastecimiento públicos y privados durante el manejo del agua. Procedimientos sanitarios para el muestreo de agua. Diario Oficial de la Federación. 1 de agosto de 2003.
Norma Mexicana NMX-AA-113-SCFI-2012 Análisis de agua para determinación de huevos de helminto. Diario Oficial de la Federación. 9 de abril de 2013.
Norma Mexicana NMX-AA-132-SCFI-2016. Muestreo de suelos para la identificación y la cuantificación de metales y metaloides, y manejo de la muestra. Diario Oficial de la Federación. 06 de marzo de 2017.
Ojha SC, Jaide C, Jinawath N, Rotjanapan P, Baral P. 2014. Geohelminths: public health significance. J Infect Dev Ctries. 15;8 (1):5-16.
OIE (Organización Mundial de Sanidad Animal). 2019. Código Sanitario para los Animales Terrestres 2019. ed. 28.
OIE (Organización Mundial de Sanidad Animal). 2015. Enfermedades de los animales silvestres. Hoja informativa. Versión en línea: goo.gl/UKYMU4.
Olivas, E., Flores, J., Di Giovanni, G., Corral, B., Osuna, P. 2013. Contaminación fecal en agua potable del Valle de Juárez. Terra Latinoamericana 31: 135-143.
Olmo, C., Tamayo, Y., Ayala, M., Saraboza, S. 2015. Influencia del tipo de piso (cemento vs tierra) en la incidencia de ascaridiasis en pollitas ponedoras comerciales Revista Granma Ciencia. Vol.20. Núm. 1.
OMS (Organización Mundial de la Salud). 2004. Guía integrada de parasitología sanitaria. Datos de publicación. Amman – Jordan: Organización Mundial de la Salud, Centro Regional de la OMS para actividades de salud ambiental; 2004.
OPS (Organización Panamericana de la Salud), OMS (Organización Mundial de la Salud). 2018. Indicadores de salud. Aspectos conceptuales y operativos. Washington, D.C.: OPS; 2018.
OPS (Organización Panamericana de la Salud). 2020. Medios auxiliares para el diagnóstico de las parasitosis intestinales. Washington, D.C
PANAFTOSA (Centro Panamericano de Fiebre Aftosa), OPS (Organización Panamericana de la Salud) y OMS (Organización Mundial de la Salud). 2017. Manual veterinario de toma y envío de muestras: manual técnico. Disponible en: https://iris.paho.org/bitstream/handle/10665.2/34527/01016970MT13spa.pdf?seqence=1&isAllowed=y. Fecha de consulta 18 mayo 2020.
Polo, L. 2006. Determinación de la contaminación de los suelos de los parques públicos de la localidad de Suba, Bogotá D.C. con nematodos gastrointestinales de importancia zoonótica. Tesis Maestría en Ciencias de la Salud Pública. Universidad Nacional de Colombia. Bogotá, Colombia.
Ratanapob, N., Arunvipas, P., Kasemsuwan, S., Phimpraphai, W., Panneum, S. 2012. Prevalence and risk factors for intestinal parasite infection in goats raised in Nakhon Pathom province, Thailand. Trop. Anim. Health Prod. 44(4):741–745.
Rodríguez, M. (2004). Evaluación del efecto del efecto desparasitante natural, contra nematodos de aves de traspatio, comparado con un desparasitante comercial, en la aldea el paraíso, municipio de Palencia, Guatemala. Tesis de Licenciatura, USAC, Guatemala.
Rueda, F. 2020. Rediseño de bebedero de agua para aves de corral con un sistema de filtro que reduzca el material particulado y sólidos en suspensión que contrae el agua en el ambiente externo de la zona rural del municipio de Palermo – Huila. Informe Final de Licenciatura. Universidad Cooperativa de Colombia. Neiva, Colombia.