Número:
- Vol. 3
- Num. 17
- Septiembre - Octubre
Porcicultura.com
Autores:
 Isis Yayoi
Isis Yayoi Martínez Velasco
Nacionalidad: Mexicana
Grado académico: Maestría en Ciencias Agropecuarias
 Adelfa del Carmen
Adelfa del Carmen García Contreras
 Fernando
Fernando Aguirre Acevedo
 Jesús Alberto
Jesús Alberto Guevara González
 Yasmin Guadalupe
Yasmin Guadalupe De Loera Ortega
ISSN-e:
2992-7293
Evaluación del comportamiento productivo y peso de órganos de lechones lactantes alimentados con distintas fuentes de zinc
INTRODUCCIÓN
Durante las etapas de rápido crecimiento, los cerdos requieren de nutrientes suficientes, controlados y balanceados para tener un buen desarrollo, uno de ellos es el Zinc (Zn), el cual es un micromineral presente en la mayoría de las células del organismo, desempeñando funciones estructurales, catalíticas y reguladoras (Ghaffari y Arabyaghuobi, 2018). Se ha identificado que el nivel de Zn en sangre está relacionado con el centro de la saciedad, comprometiendo el consumo de alimento y la tasa de crecimiento, así como, con la integridad intestinal y su capacidad de absorción de nutrimentos (Zhou et al., 2004; Ciria y Villanueva, 2005; De la Guardia et al., 2011; Sámano et al., 2013; Siam, 2013). Cousins et al. (2006) mostraron que el Zn tiene una retención mayor en el organismo, cuando el animal se encuentra en la etapa de crecimiento, que, durante la etapa de desarrollo, sin embargo, esto está sujeto a la biodisponibilidad de la fuente mineral, la genética y salud del animal, etapa fisiológica-productiva, condiciones ambientales y de manejo en donde estén alojados, y el sistema de producción al que estén sometidos (García-Contreras et al., 2012). Estudios realizados por Lu et al. (2018), informan que los órganos viscerales se desarrollan relativamente temprano en comparación con el desarrollo del peso corporal total. Lo cual se asocia a la capacidad de sostener un crecimiento rápido y eficiente de los animales. Por ello, el objetivo de la investigación fue identificar el efecto de fuentes orgánicas e inorgánicas de Zn en indicadores productivos y peso de órganos de lechones en etapa de lactancia.
MATERIALES Y MÉTODOS
Se evaluaron 16 camadas de lechones lactantes, desde su nacimiento [PV=1.55 kg + 0.03 (P=0.61)] hasta el destete (28 días). Los lechones se identificaron individualmente, al 3er. día de vida les fue aplicado 1 ml de hierro dextrano (Fe) (200 mg ml-1). A cada camada (C) le fue asignado aleatoriamente un tratamiento (T) experimental: T1= Dieta Base (DB) sin adición de Zn [Zn= 25 ppm]; T2= DB + 80 ppm de Zn (ZnO); T3= DB + 80 ppm de Zn (Pro-Zn); y T4= DB + 80 ppm de Zn (Met-Zn). La DB fue balanceada de acuerdo con los requerimientos nutricionales de FEDNA (2013). Cada T tuvo 4 C (repeticiones), a las que se le suministró una dieta, asegurando que con el sistema “poco y frecuente” tuvieran alimentación ad libitum. El alimento rechazado o sobrante se pesó cada 24 horas, evaluando con ello el consumo diario por camada (CDA). El agua fue suministrada a través de un bebedero de chupón. Los lechones se pesaron al inicio (PI) de la fase experimental y posteriormente cada semana (PV), para ello se utilizó una báscula electrónica. Se calculó la ganancia de peso semanal (GDPS) y conversión alimenticia (CA) hasta el final de la lactancia (Peso Final=PF). Una vez finalizado el periodo de 28 días de T, los lechones fueron destetados y pesados, posteriormente se eligieron al azar dos lechones por C, obtenido un total de 8 lechones por T (8 T-1), fueron sacrificados de acuerdo con la NOM-033-SAG/ZOO-2014. Para el peso de los órganos (PO) se utilizó una báscula digital. Los datos obtenidos se analizaron para corroborar los supuestos de normalidad y homogeneidad de la varianza del modelo, mediante las pruebas de Shapiro-Wilks y Bartlett, así como, una prueba de medias de Tukey, y un análisis de correlación (r). Se ingresaron los datos al paquete estadístico de SAS (SAS, 2003), considerando una Probabilidad (P=F) significativa a partir de P<0.05.
El cálculo del índice de órganos se realizó por medio de la fórmula utilizada por Huang et al., 2020: Índice de órganos (%) = Peso Fresco del Órgano (g) / Peso Vivo (g) × 100.
RESULTADOS
EVALUACIÓN DEL COMPORTAMIENTO PRODUCTIVO
Peso vivo (PV)
El peso promedio al nacimiento de los lechones incluidos en el experimento fue de 1.55 kg + 0.03 (P=0.61). En la Gráfica 1, se observa que no existieron diferencias entre tratamientos (P=0.37; EEM=0.318), al examinar los tratamientos a lo largo del tiempo (Tratamiento*Tiempo) se identificó que no existieron diferencias en el PV de los lechones durante la fase experimental (P=0.86; EEM=0.318).
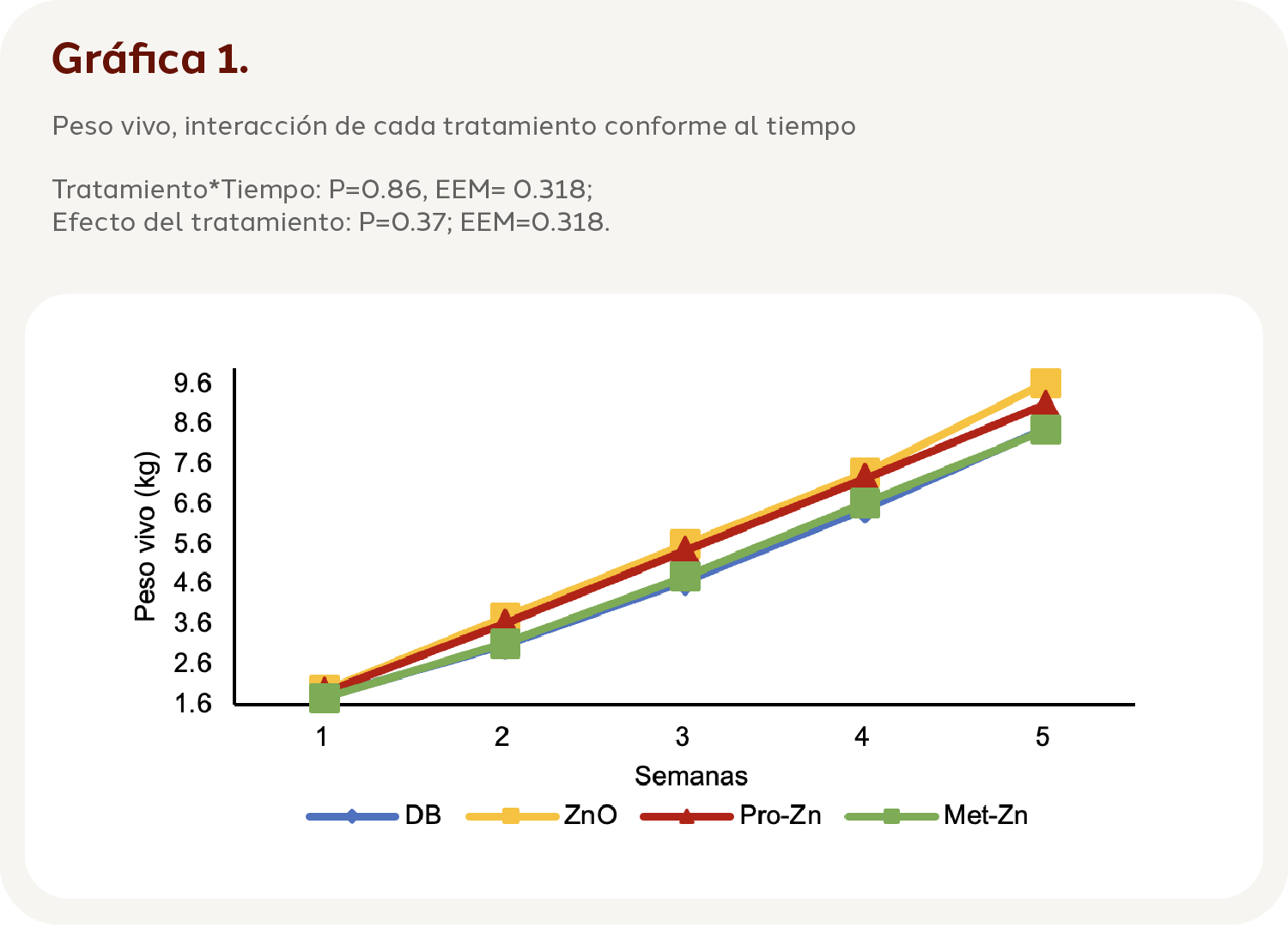
Ganancia de peso semanal
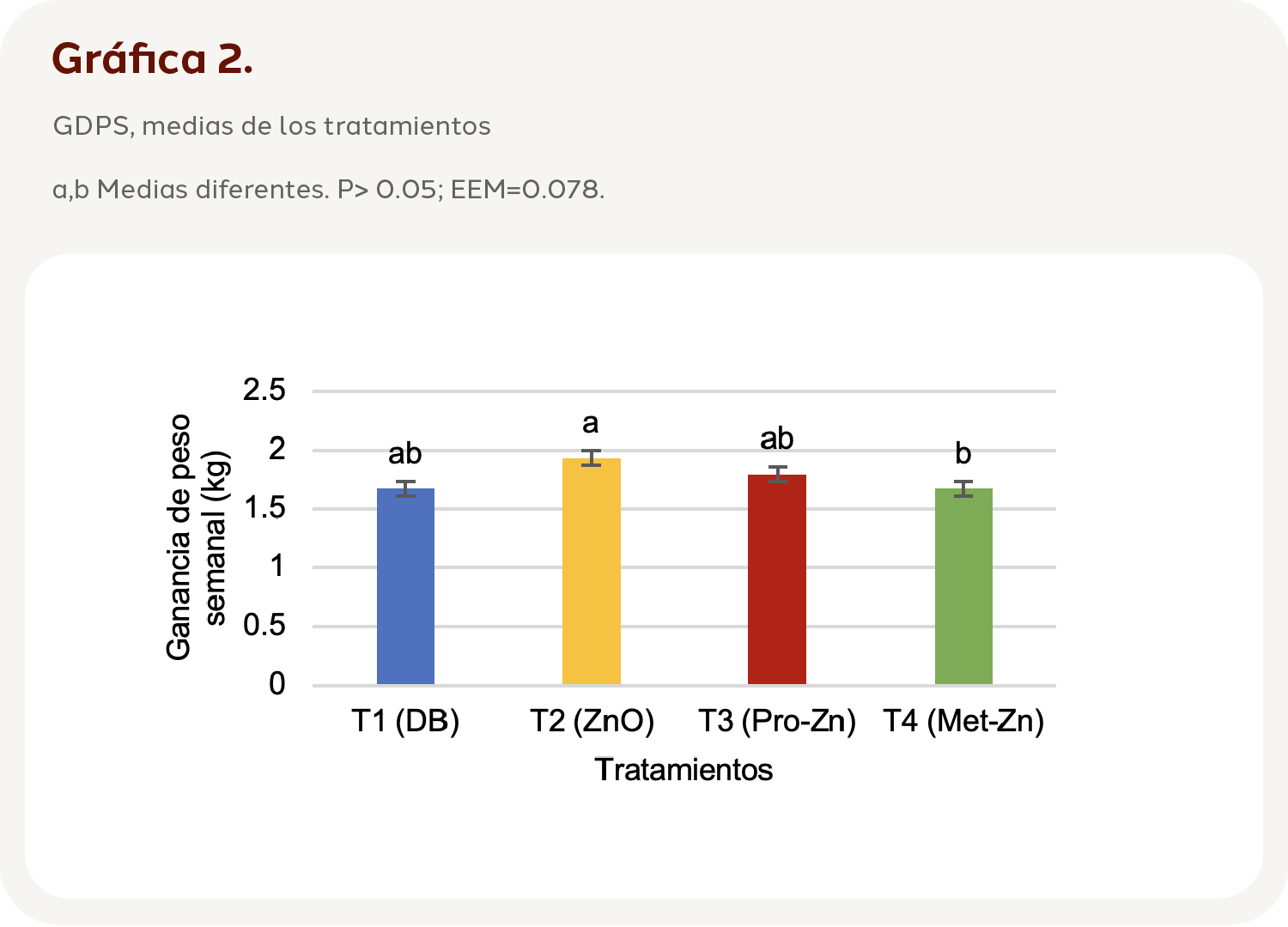
La GDPS mostró diferencias (P=0.05, EEM=0.078) entre los tratamientos T2 y T4. Aunque en el caso de los tratamientos T1 (1.67 Kg) y T3 (1.79 Kg), no existió diferencia (P=0.39; EEM= 0.19) (Gráfica 2).
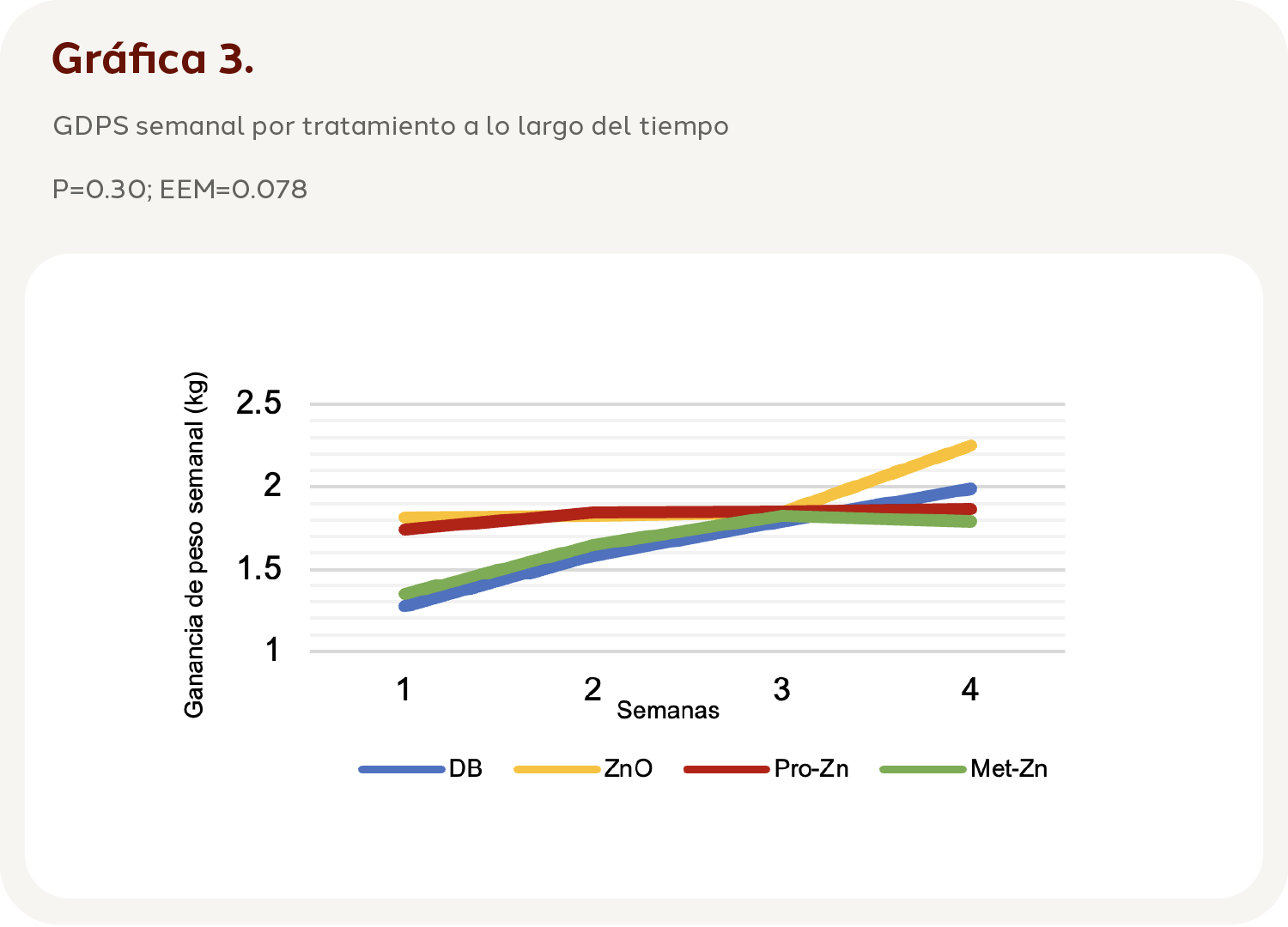
Al analizar el efecto de los tratamientos a lo largo del tiempo (Tratamiento*Tiempo), se encontró que el comportamiento no cambio en el tiempo (P=0.30). Aunque, en la semana tres se encontró que los tratamientos mostraron una GDPS similar (P=0.99) en los cuatro tratamientos, y a partir de ahí se observa como el tratamiento T2 generó una diferencia de 270 g con respecto al T1 y hasta 460 g con el T4 (Gráfica 3).
Consumo de alimento diario
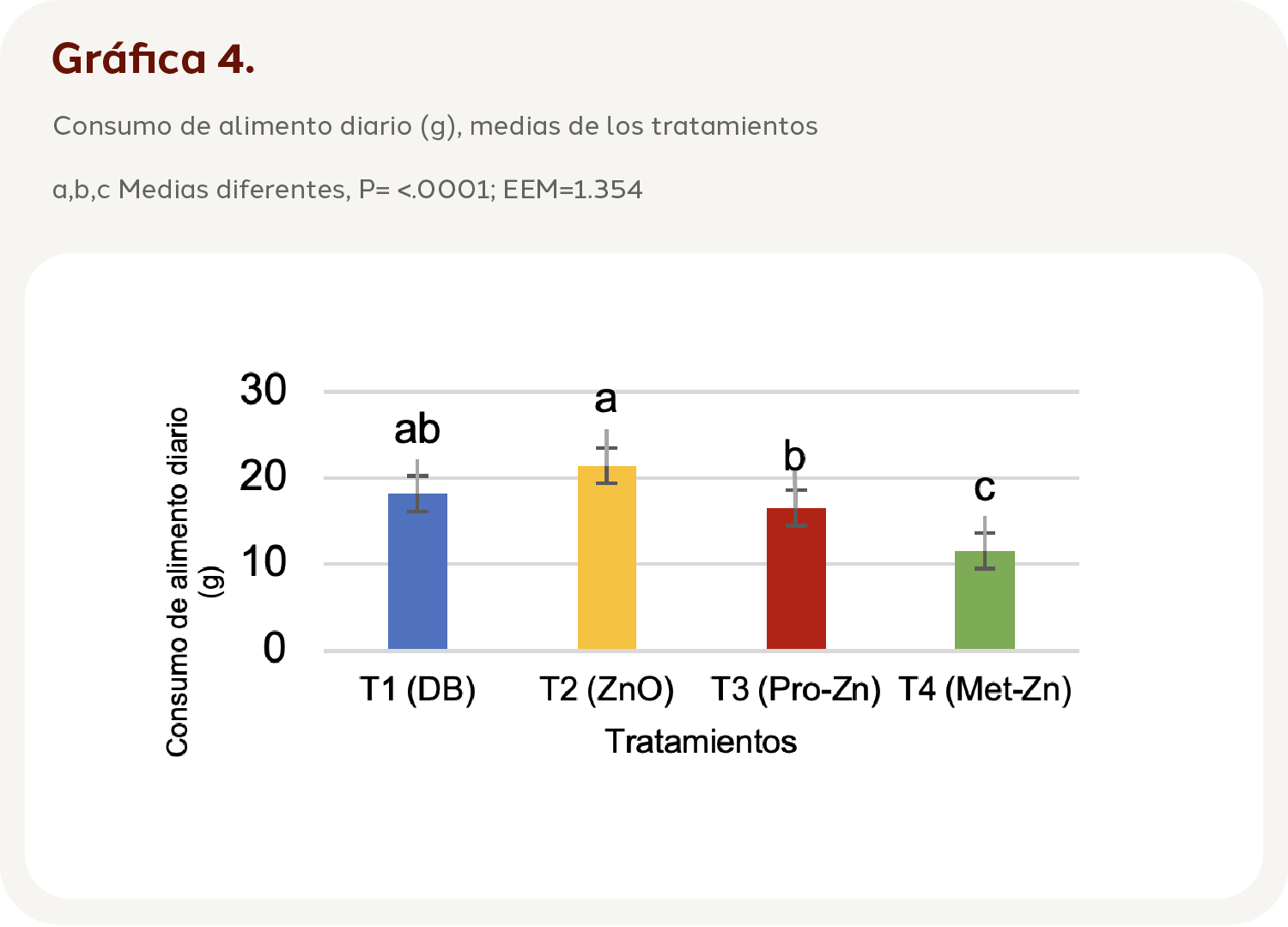
El consumo de alimento diario mostró diferencias entre tratamientos (P=<.0001; EEM=1.354), ya que el T4 tuvo un consumo de alimento menor (11.58 g) a los tratamientos T1, T2 y T3 (Gráfica 4) y el tratamiento T3 también fue diferente al T2, ya que esté ultimo mostró consumos superiores (21.49 g).
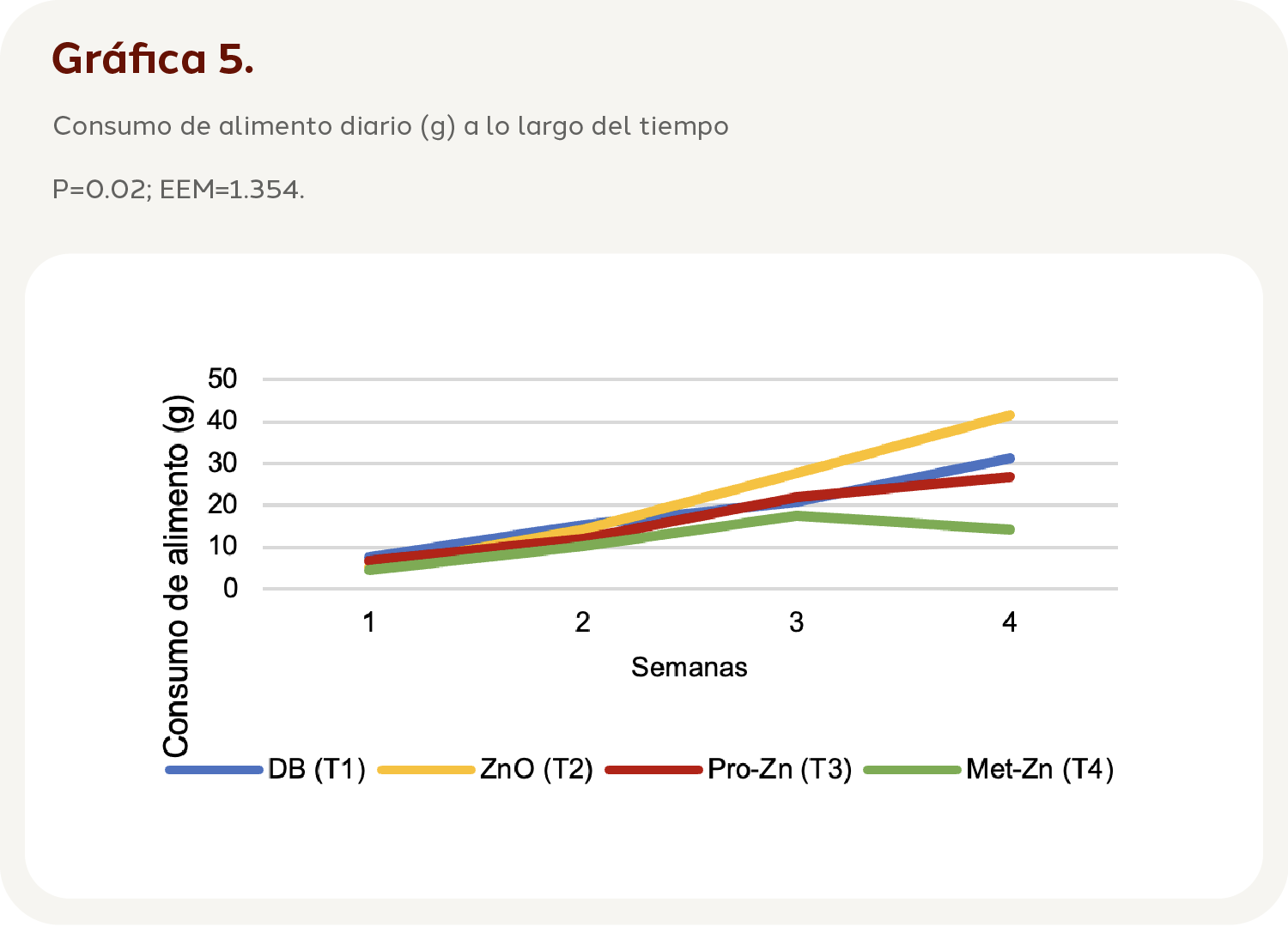
Al observar la interacción de los tratamientos a lo largo del tiempo (Tiempo*Tratamiento), se pudo identificar que fue significativa (P=0.02; EEM=1.354), el T2 fue el tratamiento que obtuvo el valor más alto al final del experimento (46.25 g), mientras que el T4 fue el que obtuvo el valor final más bajo (10.5 g) (Gráfica 5).
Conversión alimenticia
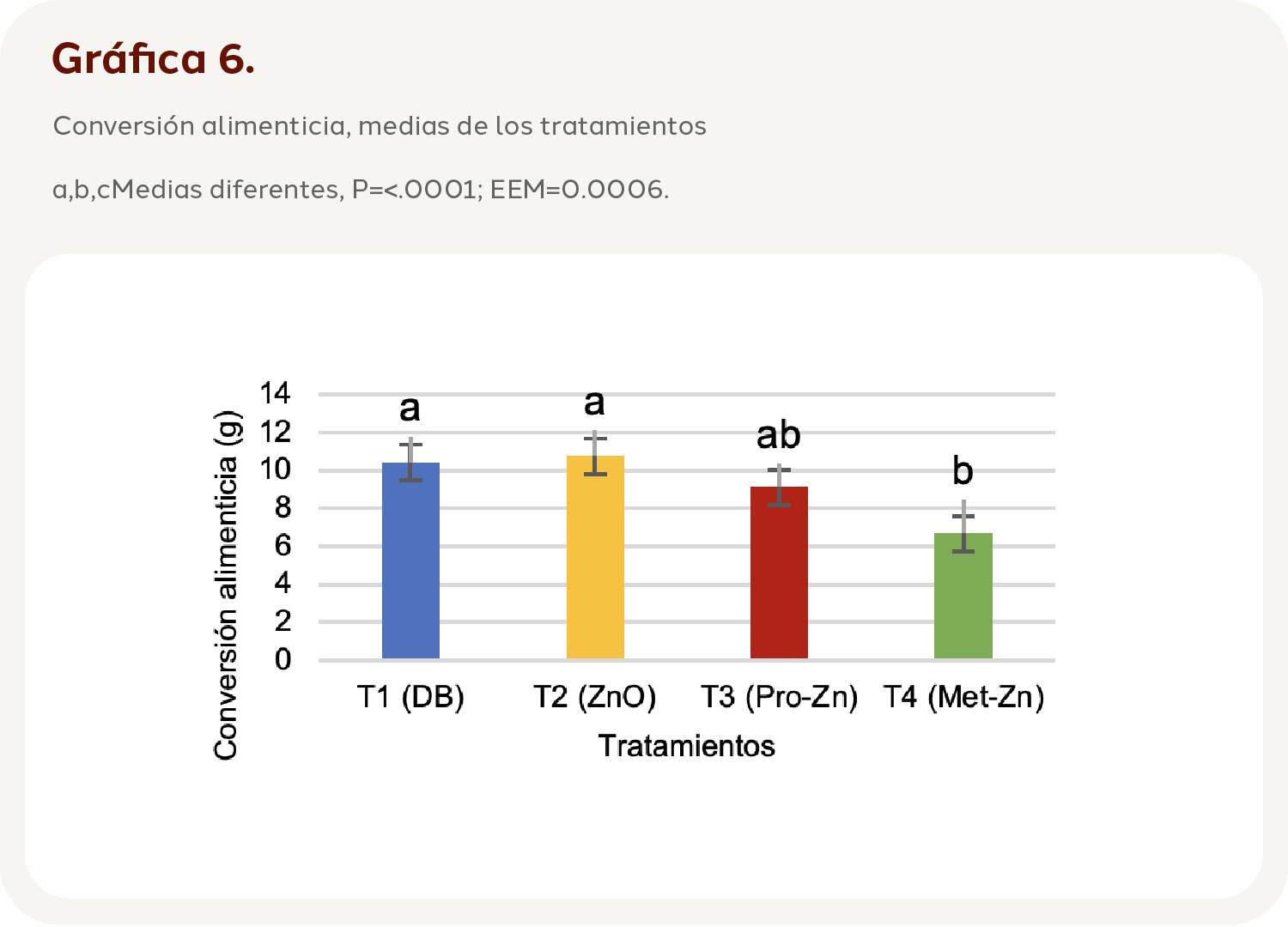
La conversión alimenticia mostró diferencias entre tratamientos (P=<.0001; EEM=0.0006). El T1 (10.42 g) fue igual que T2 (10.76 g) y T3 (9.12 g), mientras que T4 (6.68 g) fue menor y por tanto distinto a los demás tratamientos (Gráfica 6).
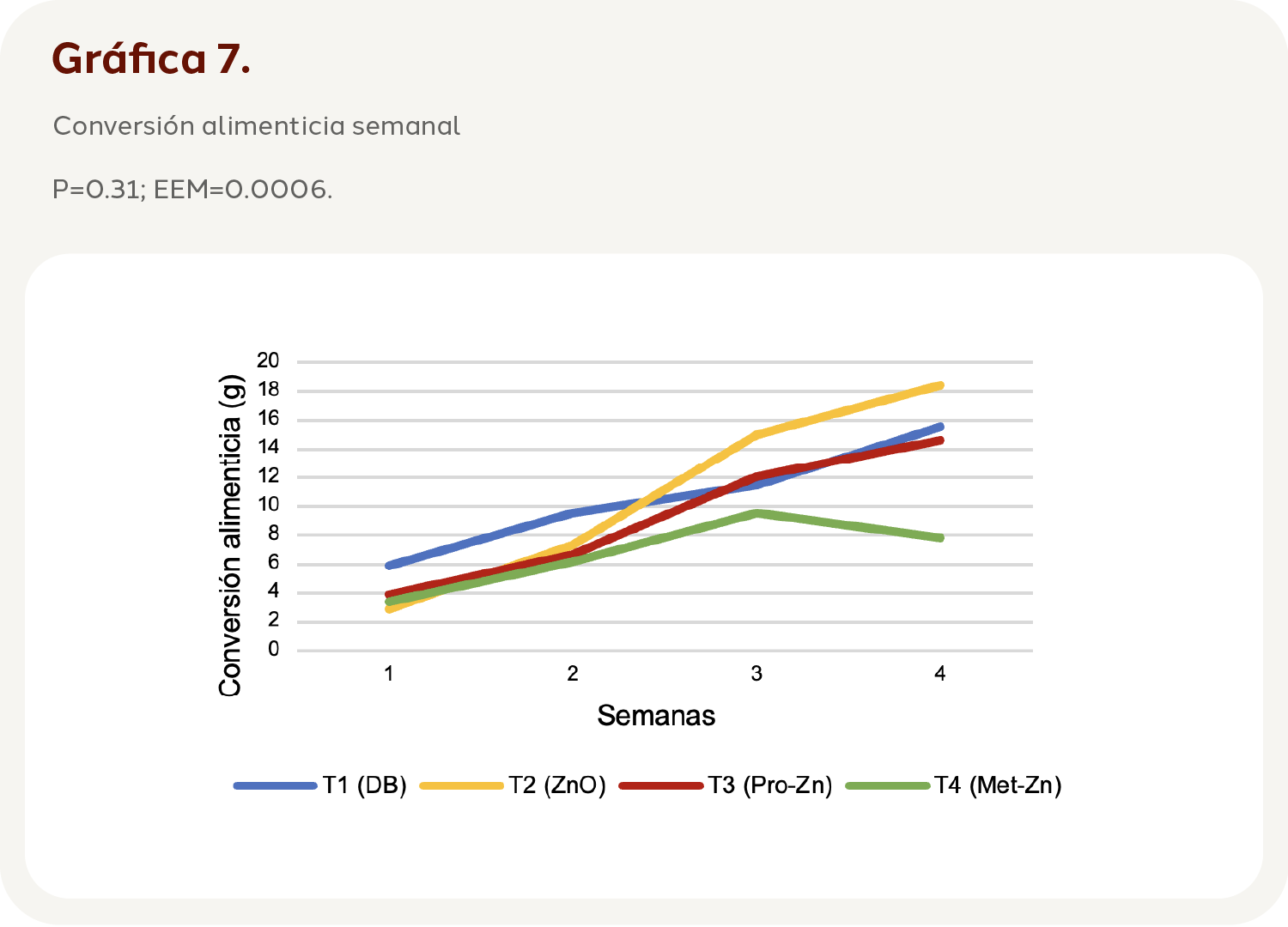
Por su parte, la conversión alimenticia al ser analizada a través del tiempo (Tratamiento*Tiempo), no fue significativa (P=0.31, EEM=0.0006) (Gráfica 7), lo cual indica que el comportamiento del tratamiento no cambió a pesar del tiempo que duró el experimento.
PESO DE LOS ÓRGANOS
En el cuadro 2 se muestran las medias de mínimos cuadrados del peso de los órganos evaluados:
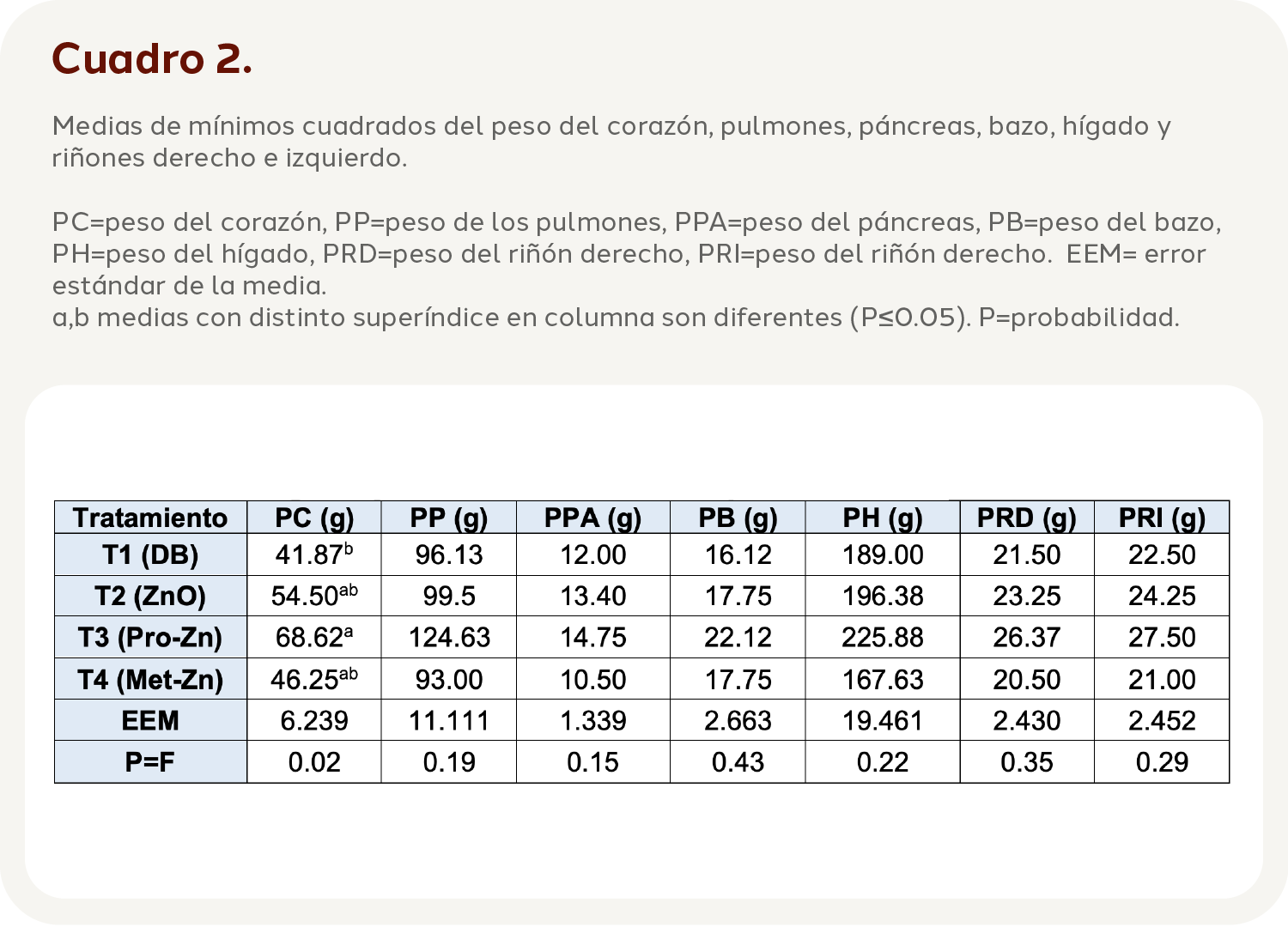
El PC mostró que el tratamiento T3 propició el mayor peso (68.62 g), en tanto que en los lechones tratados con T1 el corazón pesó 41.87 g (P=0.02; EEM= 6.239), en general, se observó que el tratamiento T3 produjo un aumento de peso de 26.75 g. Respecto al PP, no mostró diferencias entre tratamientos (P=0.19; EEM=11.111). El PPA no mostró diferencias (P=0.15; EEM=1.339), pero a pesar de que no contó con diferencias (P>005), el peso fue de 10.50 g a 14.75 g (Cuadro 2). La evaluación al PB no arrojó diferencias entre tratamientos (P=0.43; EEM=2.663) (Cuadro 2). El PH no mostró diferencias entre tratamientos (P=0.22; EEM=19.461), en el Cuadro 2 se identifica que el peso fue de 167.63 a 225.88 g. Respecto al PRD, éste no mostró diferencias (P=0.35; EEM=2.430), y el intervalo de valor de este órgano fue de 20.5 g a 26.37 g (Cuadro 2). El PRI no mostró diferencias significativas entre tratamientos (P=0.29; EEM=2.452).
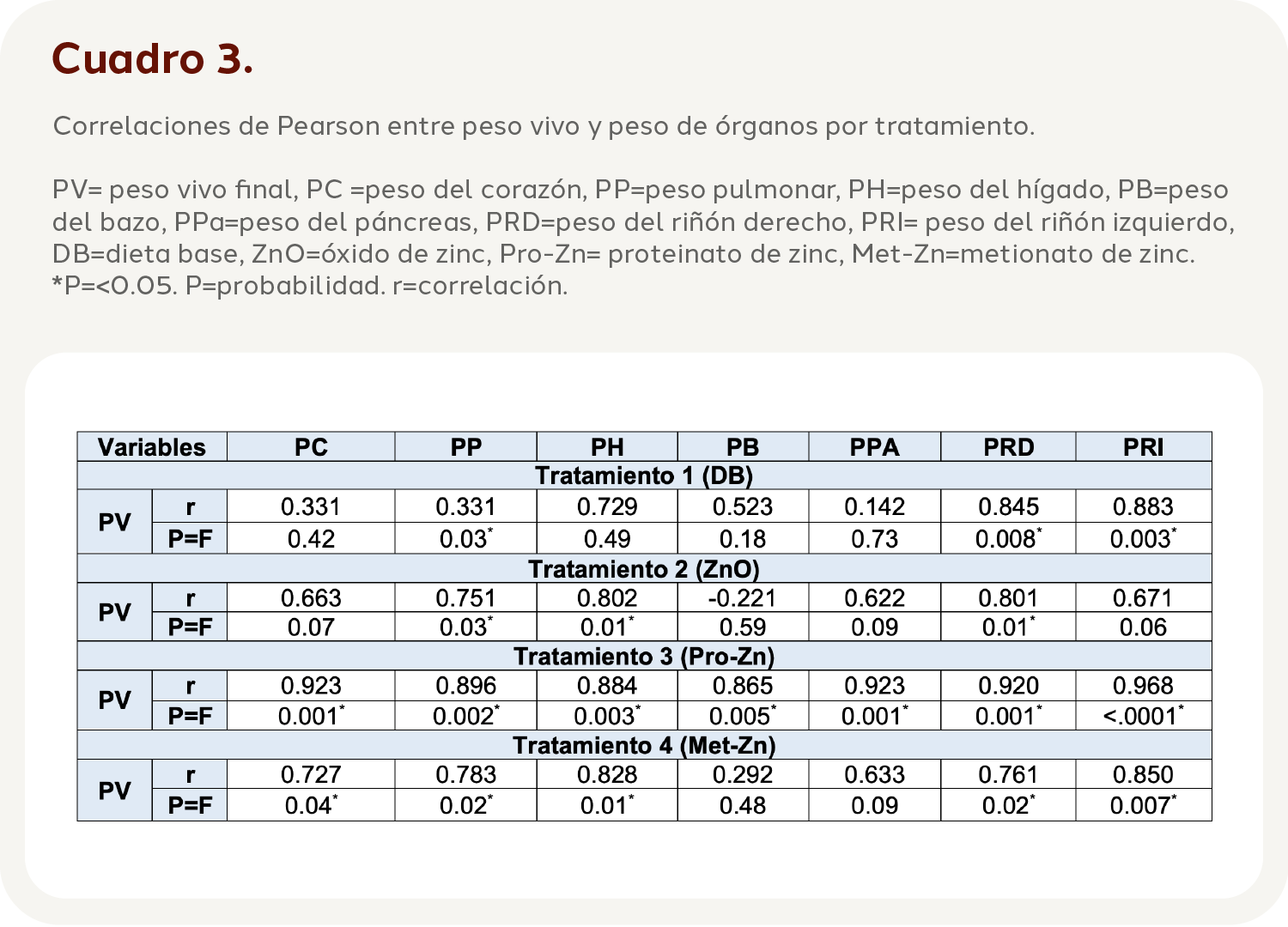
Correlaciones de Pearson entre pesos de los órganos y peso vivo de los lechones
En el Cuadro 3 se observan las correlaciones de Pearson entre peso vivo (PV) y PC, PP, PH, PB, PPA, PRD y PRI.
La correlación entre PV y PP fue positiva y significativa (P<0.04) en todos los tratamientos, en el caso del PV y el PRD/PRI se observó que existía una correlación positiva y significativa (P<0.01) en el tratamiento T1 y T3, pero para el caso del tratamiento T2 y T4 sólo existió una correlación positiva y significativa (P<0.02) con el PRD. Con respecto al PH sólo se observó una correlación positiva con el PV, en todos los tratamientos (P<0.01), exceptuando al tratamiento T1.
En el tratamiento T3 se puede detallar que existe una correlación significativa entre el PV con todos los pesos de los órganos evaluados, PC (P=0.001), PP (P=0.002), PH (P=0.003), PB (P=0.005), PPA (P=0.001) y PRD/PRI (P=0.001; P<0.0001). En el tratamiento T4 se puede resaltar que existe una correlación significativa entre el PV con el PC (P=0.04), PP (P=0.02), PH (P=0.01) y PRI (P=0.02; P=0.007) y PRD (P=0.02).
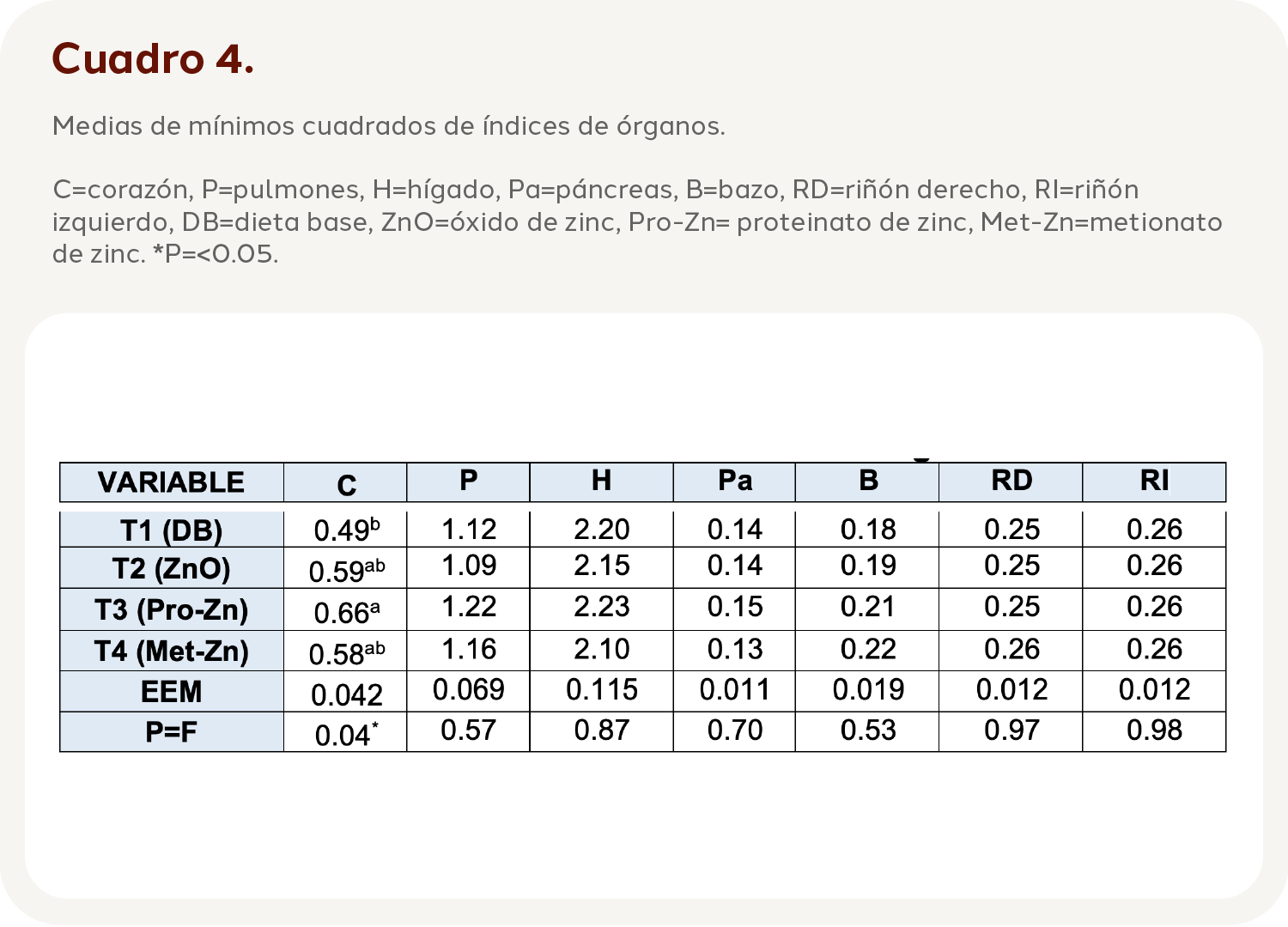
Índice de órganos
En el Cuadro 4 se observa el valor de los índices de órganos (IN), para ello se utilizó el PC, PP, PH, PB, PPA, PRD, PRI y PV. Se identificaron diferencias en el IN del corazón, entre el tratamiento T1 y T3, con 0.49 y 0.66 respectivamente (P=0.04). En el caso de los demás órganos no se observaron diferencias (P>0.05) entre tratamientos, pero es de destacar que las fuentes orgánicas (Pro-Zn, Met-Zn) fueron las que generaron un IN mayor en los órganos.
DISCUSIÓN
Comportamiento productivo
Ninguno de los lechones sometidos a este experimento presentó signos de deficiencia de Zn, ya que Miller et al. (1968), indicaron que lechones destetados tempranamente que son alimentados con una dieta deficiente en este mineral, presentan paraqueratosis. Además, no se observaron en los animales de este experimento alguna afección en sus indicadores productivos, lo que coincide con Ruiz (2006), quien describe que animales sanos que no presenten evidencias de deficiencias nutricionales, sus indicadores productivos no se verán afectados.
Se observó que el Zn en general tuvo una influencia directa en el rendimiento del crecimiento, esto podría deberse a que se encontró en una concentración óptima en las dietas de los lechones (Abd et al., 2017). Ya que si existe una deficiencia de Zn en la dieta el consumo de alimento y ganancia de peso disminuyen (Huang, 2020). Se ha reportado que 75 ppm de Zn orgánico es necesario para los cerdos de rápido crecimiento con una composición de tejido magro muy alto (Hill et al., 2014), como el caso de los lechones del presente experimento, que fueron alimentados con 80 ppm de Zn.
Peso vivo
El peso de los lechones es muy importante para su futuro desempeño en el crecimiento, desde el nacimiento hasta la sexta semana de vida, el lechón aumenta alrededor de 7.5 veces su PV (de Souza et al., 2012).
El presente estudio mostró que el PV de lechones lactantes no se ve afectado por el uso de 80 ppm Zn, a través de ZnO, Met-Zn y Pro-Zn. Hudson et al. (2004), indicaron que no existe un impacto en el peso corporal cuando se suministran dosis por arriba de los 40 mg kg-1 en aves, sin embargo, en lechones no existe evidencia de efecto por niveles de Zn similares a los utilizados en este estudio. Es importante mencionar que aun cuando no hubo diferencias entre tratamientos, se observó que el tratamiento T2 fue el que obtuvo los pesos más altos a lo largo del experimento, alcanzando un peso promedio de 9.62 kg, lo que coincide con Stensland et al. (2015), quienes al comparar ZnO con un cinamaldehído adicionado con un complejo permeabilizante observaron que el ZnO generó el PV más alto con 13.6 kg a una edad de 35 días y 18.2 kg a los 42 días de vida, este comportamiento podría deberse a que esta fuente inorgánica es considerada la principal para mejorar el rendimiento del crecimiento (Hill et al., 2000); en caso contrario, los lechones alimentados con el tratamiento T4 mostraron que su PV siempre fue el más bajo comparado con los demás tratamientos, lo que coincide con Yan et al. (2017), quienes alimentaron a conejos con zinc orgánico e inorgánico y de los pesos más bajos destacaron los conejos que estaban alimentados con 80 mg kg-1 de Met-Zn.
Paulicks et al. (2011), mencionan que 15 mg kg-1 de Zn independientemente de su forma es suficiente para producir un rendimiento del crecimiento óptimo en lechones destetados, lo cual puede estar relacionado con esta investigación, ya que, el tratamiento T1 contenía 25 ppm de Zn, suministrada a través de los ingredientes proporcionados en la dieta, produciendo un PV promedio igual (P=0.37) al resto de los tratamientos.
Ganancia de peso, consumo de alimento y conversión alimenticia
Se observó que la GDPS fue mayor en los lechones que fueron alimentados con el tratamiento T2 (80 ppm de ZnO), con una ganancia promedio de 276.42 g diarios, lo que concuerda con Hollis et al. (2005), quienes compararon dietas de ZnO y Met-Zn, siendo el ZnO el que generó una GDPS mayor más rápidamente y de manera eficiente, también Stensland et al. (2015), al comparar una dieta con 100 mg kg-1 de ZnO contra un cinamaldehído adicionado con un complejo permeabilizante, indicaron que el ZnO genera una ganancia de peso diaria mayor con 381 g, del día 0 al 7 después del destete. Es fundamental mencionar que lechones menores a 15 días de vida tienen una mejor respuesta al crecimiento con ZnO que lechones de 20 días o más (Hill et al., 2001), lo que coincide con este experimento, ya que los lechones se estudiaron desde su nacimiento.
El tratamiento T4 fue el tratamiento que generó una menor GDPS en los lechones, con una ganancia promedio de 238.85 g diarios, esto podría deberse a la dosis baja de 80 ppm que se utilizó en este experimento, ya que Ward et al. (1996) al brindar una dosis de 250 ppm de Met-Zn observaron un aumento en el rendimiento del crecimiento de lechones destetados, incluso cuando lo compararon contra 2000 ppm de ZnO.
Se identificó que los lechones alimentados con el tratamiento T2 fueron los que tuvieron un mayor consumo de alimento (21.491 g) en comparación con los demás tratamientos, esto se puede deber a que el ZnO es considerado como un promotor del crecimiento y se considera un coadyuvante para la producción de la gowth hormone-releasing peptide (ghrelina), la cual estimula a un mayor consumo de alimento en los animales (Molist, 2002), también podría deberse al tiempo que se brinda el ZnO, ya que cuando se incrementa el tiempo de suplementación de 7 a 35 días, el consumo de alimento y la ganancia de peso tienden a aumentar en lechones destetados (Sales, 2013). Stensland et al. (2015), brindaron 100 mg kg-1 de ZnO e identificaron que se genera un consumo de alimento de 454 g/día, del día 0 al 7 después del destete, un valor mucho mayor que su contraparte, un cinamaldehído adicionado con un complejo permeabilizante.
El tratamiento T3 produce un consumo de alimento bajo (16.537 g) y los lechones del tratamiento T4 fueron aún menores con 11.583 g, lo que coincide con Liu et al. (2020), quienes suplementaron distintas fuentes de Zn (ZnSO4, Zn-Gly, Zn-Met) a 100 mg kg-1 y éstas no influyeron en la ingesta diaria promedio de alimento, caso contrario con Wen-Bin et al. (2019), quienes al comparar Met-Zn a 80 mg kg-1 con una fuente inorgánica (ZnSO4) identificaron que se observa un mejor efecto en la GDPS promedio en lechones destetados.
Se determinó que los lechones del tratamiento T2 y T1 fueron los que obtuvieron la CA más alta (10.7 g y 10.4 g), mientras que el tratamiento T4 tuvo una CA de 6.68 g, esto podría deberse a que las formas queladas de Zn pueden exhibir una mayor disponibilidad que las formas inorgánicas de Zn comúnmente utilizadas (Spears et al., 1999). Stensland et al. (2015), obtuvieron resultados distintos, ya que al suplementar 100 mg kg-1 de ZnO observaron un mejor comportamiento respecto a la CA (1.34 g) del día 0 al 7 después del destete en comparación con un cinamaldehído adicionado con un complejo permeabilizante.
Evaluación del peso de órganos
Los órganos viscerales representan sólo alrededor del 15% del peso corporal del cerdo y estos órganos estarán influenciados por la composición de la dieta (Nyachoti et al., 2000).
Los órganos evaluados en este experimento no presentaron lesiones macroscópicas que denotaran estados patológicos causados por deficiencia o toxicidad en el tejido. En algunos casos como en el de Wang et al. (2006), al suplementar 5 g kg-1 de nano Zn por PV en ratones se observaron lesiones graves en los riñones y estómago.
Es importante resaltar que la biodisponibilidad juega un papel crucial para el aprovechamiento de los minerales, ya que indica la cantidad de un mineral que se absorbe y es utilizado por el animal (Ghaffari y Arabyaghuobi, 2018), la biodisponibilidad del Zn en la dieta dependerá de la fuente utilizada (García, 2010), existen grandes variaciones entre las fuentes orgánicas e inorgánicas (Liu et al., 2014). En este estudio se pudo identificar que el tratamiento T3 fue el tratamiento que propició un mayor peso en los órganos viscerales, esto podría deberse a que el Pro-Zn es un mineral orgánico y con una biodisponibilidad del 100% (TBCyA, 2017), lo que indica que esta fuente orgánica cumple con las características fisicoquímicas necesarias para garantizar una buena estabilidad en el organismo.
Corazón: en el caso de los lechones de este estudio se observaron diferencias entre tratamientos, siendo el tratamiento T3 el que arrojó el índice del corazón más alto con 0.66, lo que supera los índices obtenidos por Huang et al. (2020), quienes en ratas observaron que brindar 13 mg kg-1 de Zn, 38 mg kg-1 ZnSO4 y 2 mg kg-1 de Bacillus subtilis-Zn genera índices de 0.43 a 0.45, mientras que 17 y 32 mg kg-1 de Bacillus subtilis-Zn genera índices de 0.49 a 0.54.
Pulmones: en este experimento el índice del órgano pulmón más alto lo obtuvo el tratamiento T3 con 1.22, lo que evidencia valores superiores a los publicados por Huang et al. (2020), quienes suministraron 17 mg kg-1 de Bacillus subtilis-Zn a ratas y observaron que se genera un índice en los pulmones de 0.82 y 2 mg kg-1 de Bacillus subtilis-Zn generan 0.76.
Páncreas: los resultados obtenidos de este experimento indican que el índice más alto lo obtuvo el tratamiento T3 con un valor de 0.15, los lechones utilizados en este estudio son considerados de alta eficiencia, por lo cual podría deberse que el peso del páncreas se relacione con la eficiencia del animal, un animal de alta eficiencia tendrá un páncreas de mayor masa en comparación con un animal que posea una baja eficiencia (Meyer et al., 2015). van Heugten et al. (2003), compararon ZnSO4, Lys-Zn y Met-Zn y los pesos más altos fueron obtenidos con 80 ppm de Met-Zn, lo que podría indicar que las fuentes orgánicas de Zn generan un mayor peso en comparación con las inorgánicas, lo que concuerda con este estudio, además coincide con Shinde et al. (2006), quienes alimentaron a cobayos con distintas fuentes de Zn y la que generó un mayor índice fue 20 ppm de ZAAC (ZnCl2+Met-Zn), con un valor de 0.39.
Cuando un alimento es consumido por el lechón en gran cantidad y además este alimento posee un alto valor energético, se produce un mayor crecimiento del páncreas e hígado ya que estos órganos consumen 50% aproximadamente de la energía total (de Souza et al., 2012).
El páncreas depende más de la estimulación enteral para su crecimiento y desarrollo, que de otros estímulos (de Souza et al., 2012). Cuando el consumo de alimento se incrementa, la tasa de crecimiento del tejido pancreático lo hace de igual manera (de Souza et al., 2012). Por lo que el desarrollo pancreático está directamente relacionado con el tipo de dieta que consuma el animal, ya que, si los animales tienen acceso a alimentos ricos en proteínas, grasas o carbohidratos, este órgano tendrá que desarrollar sus funciones de acuerdo con dichos sustratos (Pluske et al., 1997).
Hígado: en ratas se observó que brindar 2 mg kg-1 de Bacillus subtilis-Zn genera un índice en el hígado de 3.14 (Huang et al., 2020), en este estudio se obtuvieron valores bajos respecto a los antes mencionados, con un índice de 2.23 que se consiguió con el tratamiento T3, lo que concuerda con Shinde et al. (2006), quienes indicaron que brindar 20 ppm de ZAAC (ZnCl2+Met-Zn) produce un índice alto (3.88) en comparación con otras fuentes. Respecto al peso del hígado, se obtuvo un valor de 225.88 g con el tratamiento T3, lo que contradice a van Heugten et al. (2003), quienes observaron que suministrar 160 ppm de ZnSO4 a lechones destetados desencadena un mayor peso en este órgano (873 g), en comparación con fuentes orgánicas (Met y Lys).
Es importante mencionar que el hígado es el principal órgano de almacenamiento de Zn y es el órgano que más responde a la función antioxidante y es sensible a la deficiencia de Zn (Wang et al., 2010; She et al., 2017).
Bazo: en el presente estudio los lechones alimentados con el tratamiento T4 obtuvieron el índice más alto, con un valor de 0.22, lo que es bajo comparado con lo obtenido por Huang et al. (2020), quienes suministraron 17 mg kg-1 de Bacillus subtilis-Zn y obtuvieron un índice de 0.38; pero fue alto en comparación con Shinde et al. (2006), quienes observaron que al brindar 50% y 50% de 20 ppm de ZnSO4 y ZAAC (ZnCl2+Met-Zn) se obtiene un índice de 0.17 en cobayos; esto puede deberse a que el peso del bazo sugiere un mayor o menor volumen sanguíneo (Cesta, 2006).
En el caso del bazo el peso más alto lo obtuvo el testigo (80 ppm de ZnSO4). En ningún órgano hubo diferencias entre tratamientos (van Heugten et al., 2003).
Riñones: los lechones de este experimento presentaron el mayor índice con el tratamiento T4 con un valor de 0.26, lo que es muy bajo a lo obtenido por Huang et al. (2020), quienes en ratas brindaron 2 mg kg-1 de Bacillus subtilis-Zn y esto generó un índice 0.98 y con 38 mg kg-1 de ZnSO4 generó 0.87.
CONCLUSIONES
El consumo de 80 ppm de Zn a través de la fuente inorgánica ZnO mejora el PV, la GDPS, el CDA y la CA de lechones lactantes. El uso de 80 ppm Zn, incluyendo el Pro-Zn en la dieta de lechones lactantes, incrementa significativamente el peso del corazón, y se observa un peso superior en pulmones, páncreas, bazo, hígado y riñones, lo que podría ser un indicador de un desarrollo productivo adecuado para las exigencias del mercado nacional actual.
RECOMENDACIONES
Alimentar con una concentración de Zn de acuerdo con la edad, etapa fisiológica-productiva, genética y finalidad zootécnica, implementando programas de alimentación que disminuyan la excreción de minerales será positivo para el medio ambiente y además contribuirá al bienestar de los animales, para el sostenimiento de la producción porcina en el futuro.
REFERENCIAS
- NORMA OFICIAL MEXICANA NOM-117-SSA1-1994, Bienes y servicios. Método de prueba para la determinación de cadmio, arsénico, plomo, estaño, cobre, fierro, zinc y mercurio en alimentos, agua potable y agua purificada por espectrometría de absorción atómica.
- Ghaffari M., Arabyaghoubi M. 2018. Zinc as an essential nutritional component of human body: a systemic review. International Journal of Pharmaceutical & Biological Archives. 9 (2):62-65.
- FEDNA (Fundación Española para el Desarrollo de la Nutrición Animal). 2013. Necesidades nutricionales para ganado porcino: Normas FEDNA. Madrid, España. Pp. 114.
- SAS. 2003. Statistical Analysis System. SAS Release 9.1 for Windows, SAS Institute Inc.Cary, NC, USA.
- Ren, P., Chen, J., Wedekind, K., Hancock, D., & Vázquez-Añón, M. (2020). Interactive effects of zinc and copper sources and phytase on growth performance, mineral digestibility, bone mineral concentrations, oxidative status, and gut morphology in nursery pigs. Translational Animal Science, 4(2), 783-798.
- Hill, G. M., & Shannon, M. C. (2019). Copper and zinc nutritional issues for agricultural animal production. Biological Trace Element Research, 188(1), 148-159.
- Molist F. & R. Davin. 2002. Utilización de Óxido de Zinc en lechones. Web site:
http://albeitar.portalveterinaria.com/noticia/11972/Articulosporcino/Utilizacion-del-oxido-de-cinc-en-lechones-para-el-control-de -la-diarrea-posdestete.html.
- HUDSON B.P., FAIRCHILD B.D. and WILSON J.L. (2004) Breeder age and zinc source in broiler breeder hendiets on progeny characteristics at hatching. Journal of Applied Poultry Research 13: 55 -64.10.1093/japr/13.1.55
- Abd El-Hack, M. E., Alagawany, M., Arif, M., Chaudhry, M. T., Emam, M., & Patra, A. (2017). Organic or inorganic zinc in poultry nutrition: a review. World's Poultry Science Journal, 73(4), 904-915.
- Hill, GM, GL Cromwell, TD Crenshaw, CR Dove, RC Ewan, DA Knabe, AJ Lewis, GW Libal, DC Mahan, GCShurson, LL Southern y TL Veum. 2000. Efectos de promoción del crecimiento y cambios plasmáticos de la alimentación con altas concentraciones dietéticas de zinc y cobre a lechones destetados (estudio regional). J. Anim. Sci. 78: 1010-1016.
- Ward, T. L., G. L. Asche. G. F. Louis, and D. S. Pollmann. 1996. Zinc-methionine improves growth performance of starter pigs. J. Anim. Sci. 74(Suppl. 1):182. (Abstr.)
- Carlson, M. S., Boren, C. A., Wu, C., Huntington, C. E., Bollinger, D. W., & Veum, T. L. (2004). Evaluation of various inclusion rates of organic zinc either as polysaccharide or proteinate complex on the growth performance, plasma, and excretion of nursery pigs. Journal of Animal Science, 82(5), 1359-1366.
- Nyachoti, C. M., De Lange, C. F. M., McBride, B. W., Leeson, S., & Schulze, H. (2000). Dietary influence on organ size and in vitro oxygen consumption by visceral organs of growing pigs. Livestock Production Science, 65(3), 229-237.
- Hollis, G. R., Carter, S. D., Cline, T. R., Crenshaw, T. D., Cromwell, G. L., Hill, G. M., ... & Stein, H. H. (2005). Effects of replacing pharmacological levels of dietary zinc oxide with lower dietary levels of various organic zinc sources for weanling pigs. Journal of animal science, 83(9), 2123-2129.
- Wang Y, Tang JW, Ma WQ, Feng J. Dietary zinc glycine chelate on growth performance, tissue mineral concentrations, and serum enzyme activity in weanling piglets. Biol Trace Elem Res. 2010; 133:325–b34.
- Huang, Y., Wang, B., Liu, G., Ge, W., Zhang, M., Yue, B., & Kong, M. (2020). Effects of Bacillus Subtilis-Zinc on Rats with Congenital Zinc Deficiency. Biological Trace Element Research, 194(2), 482-492.
- Hill GM, Mahan DC, Jolliff JS (2014) Comparison of organic and inorganic Zn sources to maximize growth and meet the Zn needs of the nursery pig. J Anim Sci 92:1582–1594. https://doi.org/10.2527/jas.2014-8173.
- Cesta MF. Normal structure, function, and histology of the spleen Toxicol. Pathol., 34 (2006), pp. 455-465.
- TBAyC (Tablas Brasileñas para Aves y Cerdos). 2017. Composición de Alimentos y Requerimientos Nutricionales. Universidad Federal de Viçosa. Brasil. Pp. 488.
- Meyer, A. M., Vraspir, R. A., Ellison, M. J., & Cammack, K. M. (2015). The relationship of residual feed intake and visceral organ size in growing lambs fed a concentrate-or forage-based diet. Livestock Science, 176, 85-90.
- She, Y., Huang, Q., Li, D., & Piao, X. (2017). Effects of proteinate complex zinc on growth performance, hepatic and splenic trace elements concentrations, antioxidative function and immune functions in weaned piglets. Asian-Australasian journal of animal sciences, 30(8), 1160.