Número:
- Vol. 3
- Num. 17
- Septiembre - Octubre
Ganaderia.com
Autores:
 Carlos Eduardo
Carlos Eduardo Aragón López
Nacionalidad: Mexicana
Grado académico: Doctor en Ciencias, Especialidad en Biotecnología
 E.S.
E.S. Aguirre Urías
 J.C.
J.C. Leyva Corona
 L. A.
L. A. Flores Encinas
 M.
M. Castro Urrea
 M.I.
M.I. Morales Pablos
ISSN-e:
2992-7293
Desarrollo de un medio de cultivo alternativo para asegurar la integridad de Tritrichomona foetus post descongelamiento de muestras positivas
Resumen
La tricomoniasis bovina es una enfermedad venérea causada por Tritrichomona foeuts. El impacto reproductivo que genera este protozoario en los sistemas de producción bovino, donde interviene la monta directa o la inseminación artificial con semen contaminado, se relaciona a una menor cosecha de becerro, heterogeneidad en grupos de partos, mayor número de vacas improductivas y altos costos por el efecto descarte-reemplazo de animales infectados independientemente de su valor genético. Algunos medios utilizados para el transporte de muestras de T foetus no protegen al parasito de la desnaturalización de los ácidos nucleicos para fines de diagnóstico molecular si se almacena o congela la muestra por largos periodos de tiempo y no se comercializan en México, lo que obstaculiza el diagnóstico. En este sentido, el objetivo del estudio fue desarrollar un medio de cultivo que asegure la integridad de T. foetus posterior al descongelamiento de la muestra. Para esto, se obtuvieron muestras de exudados de vacas con piometra procedentes de diferentes ranchos ubicados al noroeste de México. De la muestra original se extrajo el ADN para su análisis por PCR e identificar las muestras positivas a T. foetus (TRICH+). Se formuló el medio de cultivo TrichonEmma y se le añadió antibióticos. Las muestras TRICH+ fueron sembradas e incubadas en TrichonEmma. A los días 4 y 7 post siembra los tubos fueron observados por microscopia directa y se tiñeron con Giemsa. Se observó desarrollo y motilidad del protozoario a partir del 4d por microscopia y las tinciones confirmaron estructuras características de T. foetus. El medio de cultivo (TrichonEmma) desarrollado en el presente estudio logró conservar exitosamente la integridad de T. foetus, incluso la sobrevivencia y desarrollo del protozoario después del descongelamiento. Así mismo, éste estudio es el primero en México que identifica molecularmente a T. foetus a partir de piometra de vacas abortadas.
Palabras clave: Tricomoniasis, medios de transporte, sobrevivencia, descongelamiento.
Introducción
La tricomoniasis bovina es la enfermedad venérea causada por el protozoario extracelular T. foetus que está mundialmente distribuida y es endémica principalmente en regiones que utilizan la monta natural como manejo reproductivo (da Silva et al., 2020; WOAH, 2018). La infección por T. foetus puede causar pérdidas económicas significativas debido a la diminución en el rendimiento reproductivo del rebaño afectado, que van desde temporadas de parto prolongadas, menor tasa de parto, mantenimiento de ganado no productivo, pruebas de diagnóstico para el control de infecciones y hasta mayores costos como resultado del sacrificio y reemplazo del ganado infectado (Clothier et al., 2015; Ondrak, 2016; Gifford et al., 2020).
La enfermedad se transmite a las vacas adultas directamente por el coito con el toro enfermo, ya que los machos normalmente no muestran signos clínicos de infección, por lo tanto, se les considera portadores subclínicos del agente (Martin et al., 2021; Yao, 2021), lo que hace a la Inseminación Artificial (IA) una importante estrategia de prevención. Sin embargo, Trichomona foetus también se transmite mediante vaginas artificiales contaminadas o semen criopreservado de toros positivos (Burgess y McDonald, 1992). Por el contrario, las hembras infectadas, ya sea por monta natural o IA, ocasionalmente pueden cursar vaginitis, aborto, infertilidad y otros problemas reproductivos. Estos signos clínicos en la mayoría de los casos positivos se “autocuran” o desaparecen posteriormente de varias semanas o meses con reposo reproductivo. Es posible que algunas vacas queden infértil permanente o incluso la prevalencia continua del microorganismo en un pequeño por ciento, siendo necesario sacrificar hembras antes de que hayan completado una vida productiva (Michi et al., 2016; da Silva et al, 2020; Martin et al., 2021).
En algunos países se utiliza el aislamiento de T. foetus vivo para su diagnóstico por microscopia, para lo cual se utilizan diferentes medios transporte comerciales. Este método diagnostico en algunos países aún se considera el estándar de oro para el diagnóstico pese a su baja sensibilidad. Actualmente, en países desarrollados se utilizan medios de transporte comerciales combinado con la PCR y PCR tiempo real para mejorar la sensibilidad y especificidad del diagnóstico (WHOA, 2018), a diferencia de países como México donde el principal problema es el costo y la introducción de los medios de cultivo al país.
La presencia de la enfermedad fue reconocida en México desde hace más de 60 años en ganado lechero ubicado en una zona lechera del Valle de México (Cuevas, 1967). El incremento en los casos de animales con signos clínicos similares a T. foetus y la movilización de toros procedentes del vecino país, han sido una preocupación en los últimos años, por lo que su diagnóstico y control no había sido relevante hasta hace poco. Un estudio reciente al norte de México en el estado de Chihuahua (Ramírez, 2017) reporto la presencia de T. foetus en el 21.8% de los toros muestreados, en el que el 60-65% de los ranchos muestreados tuvieron al menos un animal positivo. Una tesis de maestría en el estado de Veracruz reporto una frecuencia de 36% y 14.3% de vacas y toros positivos a T. foetus (Villareal 2020). En estos estudios se utilizaron la microscopía directa de frotis en portaobjetos teñidos con Giemsa así como el sistema de diagnóstico de cultivo comercial para su uso por PCR.
El control de la tricomoniasis en México todavía se considera tarea difícil, ya que los datos disponibles de prevalencia en el país son escasos para medir la severidad de la enfermedad ya que el desarrollo y estandarización de pruebas disponibles para México está en desarrollo, así como los métodos de muestreo, reactivos y material para no depender de la importación de ellos. Un factor relevante es la capacidad de T. fetus para sobrevivir a la congelación y seguir siendo potencialmente infeccioso (Ribeiro et al., 2021). Es posible que el protozoario sobreviva al congelamiento y muestre viabilidad al posterior descongelamiento sin criopreservador si se formula un medio de transporte alternativo que complemente un sistema de diagnóstico de T. foetus. Debido a esto, el presente ensayo tuvo como objetivo desarrollar un medio de cultivo que asegurara la integridad de T. foetus posterior al descongelamiento de la muestra. Lo anterior facilitara la capacidad de obtener resultados más rápidos y a menor costo en México sin la necesidad de la importación de medios de cultivos.
Materiales y métodos
Ubicación geográfica y animales de estudio
Las muestras se recolectaron en ranchos de diferentes localidades del Estado de Sonora. Se examinaron un total de 10 vacas adultas abortadas de diferentes edades y regiones. Se recogió líquido vaginal de cada vaca después del aborto (no más de 1 semana después del aborto) utilizando una pipeta de inseminación artificial acoplada a una jeringa de 5 ml y depositada en un tubo Falcon estéril de 50 ml. Las muestras de alta viscosidad se diluyeron con 10 ml de buffer fosfato salino (Sigma-Aldrich) y se centrifugaron a 2200 x g durante 15 minutos. Se eliminó el sobrenadante y el sedimento se resuspendió nuevamente en un volumen de 1 ml. Finalmente se utilizaron 200 µl para la extracción de ADN y el resto se congelo a -60°C hasta su posterior uso.
Obtención de ácidos nucleicos a partir de piometra
Las muestras de piometra diluidas se homogeneizaron primero por agitación e inversión. A continuación, las extracciones de ADN se llevaron a cabo mediante el Sistema de extracción de ácidos nucleicos automático taco™ (GeneReach Biotechnology Corp.) utilizando el DNA/RNA Extraction Kit (taco™) de acuerdo con el método del fabricante. El producto final extraído de ácidos nucleicos fue cuantificado con espectrofotometría UV (BioSpect-Nano, Shimadzu®). La integridad del ADN extraído se verificó mediante electroforesis en un gel de agarosa al 1,5 % teñido con bromuro de etidio. Todas las extracciones se almacenaron en viales estériles de 1,5 ml a -20 °C para ser procesadas posteriormente para la técnica de PCR.
Detección molecular de T. foetus por PCR
Las muestras de ADN se analizaron mediante la reacción en cadena de la polimerasa (PCR) utilizando el conjunto de cebadores TFR3: 5'_CGGGTCTTCCTATATGAGACAGAACC-3' y TFR4: 5'-CGGGTCTTC CTATATGAGACAGAACCGGAGCTGAATG-3', amplificando una región de 347 pb del gen que codifica para el ARNr 5.8S y las regiones ITS1 e ITS2 de T. foetus (Felleisen et al., 1998). Para las reacciones se utilizó el kit precargado GoTaq® Flexi DNA Polymerase PCR (Promega) que contiene Green GoTaq®, que sirve como tampón de reacción y solución de carga de gel, lo que permite cargar las reacciones directamente para un análisis rápido y eficiente. Las reacciones se realizaron en un volumen final de 25 μl, con una concentración de 1X Green GoTaq Buffer 5x, 1.5 mM MgCl2, 0.2 mM para cada dNTP, 0.4 μM de cada cebador, 1.25 u de GoTaq DNA Polymerase, 5 μl de DNA y H2O libre de nucleasas a 25 µL. Las condiciones del análisis de PCR fueron 1 ciclo de 95 °C por 3 min, 32 ciclos de; 95 °C por 15 s, 62 °C por 30 s y 72 °C por 30 s y un paso de extensión final de 72 °C por 5 min. El producto se identificó en gel de agarosa al 1.5% con bromuro de etidio, considerando bandas positivas con el tamaño del aplicón del agente.
Desarrollo de un medio de cultivo para el crecimiento de Tritrichomona foetus (TrichonEmma)
Para la formulación del medio de cultivo se utilizó L- cistina, tioglicolato de sodio, peptona de caseína, extracto de levadura, dextrosa, NaCl, K2HPO4, KH2PO4, agar base, suspendidos en 500 ml de agua destilada, fue necesario calentar un poco la mezcla en el mechero de Bunsen para que se integren todos los ingredientes. Se ajustó el pH de 7.0-7.4 con ácido clorhídrico o hidróxido de sodio. Posteriormente se esterilizó a 121°C, 15 lb de presión por 15 minutos y se enfrió a 49°C, después, se añadieron 25 mg de amikacina, 500,000 UI de bencilpenicilina y 25 mg de fluconazol. Finalmente se distribuyó el medio de forma aséptica en tubos de vidrio estériles con tapón de rosca de 15 ml y se conservó el medio de cultivo a 4 °C hasta su uso.
Proceso de siembra en medio TrichonEmma
Una vez listo el medio TrichonEmma se descongelaron solo las muestras de piometra positivas por PCR a temperatura ambiente. En un ambiente aséptico y con el uso de micropipetas estériles, se tomaron 200 μl del precipitado de cada muestra e inmediatamente se sembrada por triplicado en el medio desarrollado. Al finalizar, cada uno de los tubos fue homogenizado mediante rotaciones lentas para no dañar las muestras. Los tubos sembrados se colocaron en gradillas y se introdujeron a una incubadora bacteriológica a 37 °C.
Evaluación del medio de cultivo TrichonEmma
Se realizó una evaluación directa al microscopio en guarda griega de una gota del precipitado de los medios de cultivo, colocando un cubreobjetos y aceite de inmersión para la observación a 100X al día 4 y 7 después del sembrado. Posteriormente, se realizaron frotis de los medios de cultivo, tomando con pipetas de 1 ml muestras del precipitado de cada medio. Se dejaron secar a temperatura ambiente y se fijaron con metanol durante 10 minutos. Después de ese tiempo, se tiñeron en un puente de tinción con Giemsa (1 parte de colorante y 20 partes de agua destilada). Estas evaluaciones se realizaron en guarda griega.
Resultados y discusión
Por medio de electroforesis se observó buena integridad de las moléculas de ADN extraídas, con una cuantificación por espectrofotometría en promedio de 58.32 ng/µl en las muestras y una pureza con la relación 260-280 OD de 1.85. Estos valores de cantidad y calidad de material genético son muy parecidos a los obtenidos por Gharban (2023), con una cantidad de 45,7 ng/μL y una calidad de 1.73, partiendo al igual que nuestro ensayo de piometra en vacas abortadas. Demostrando en ambos casos una buena cantidad de material genético y una calidad sin contaminantes derivados de guanidina, fenoles, sales caotrópicas o hidratos de carbono.
En la detección por PCR, el 20% de las vacas abortadas resultaron positivas a T. foetus (TRICH+) usando PCR convencional (Figura1), observando un bandeo especifico de la región del ADN ribosomal de T. foetus con un tamaño de 347 pb.
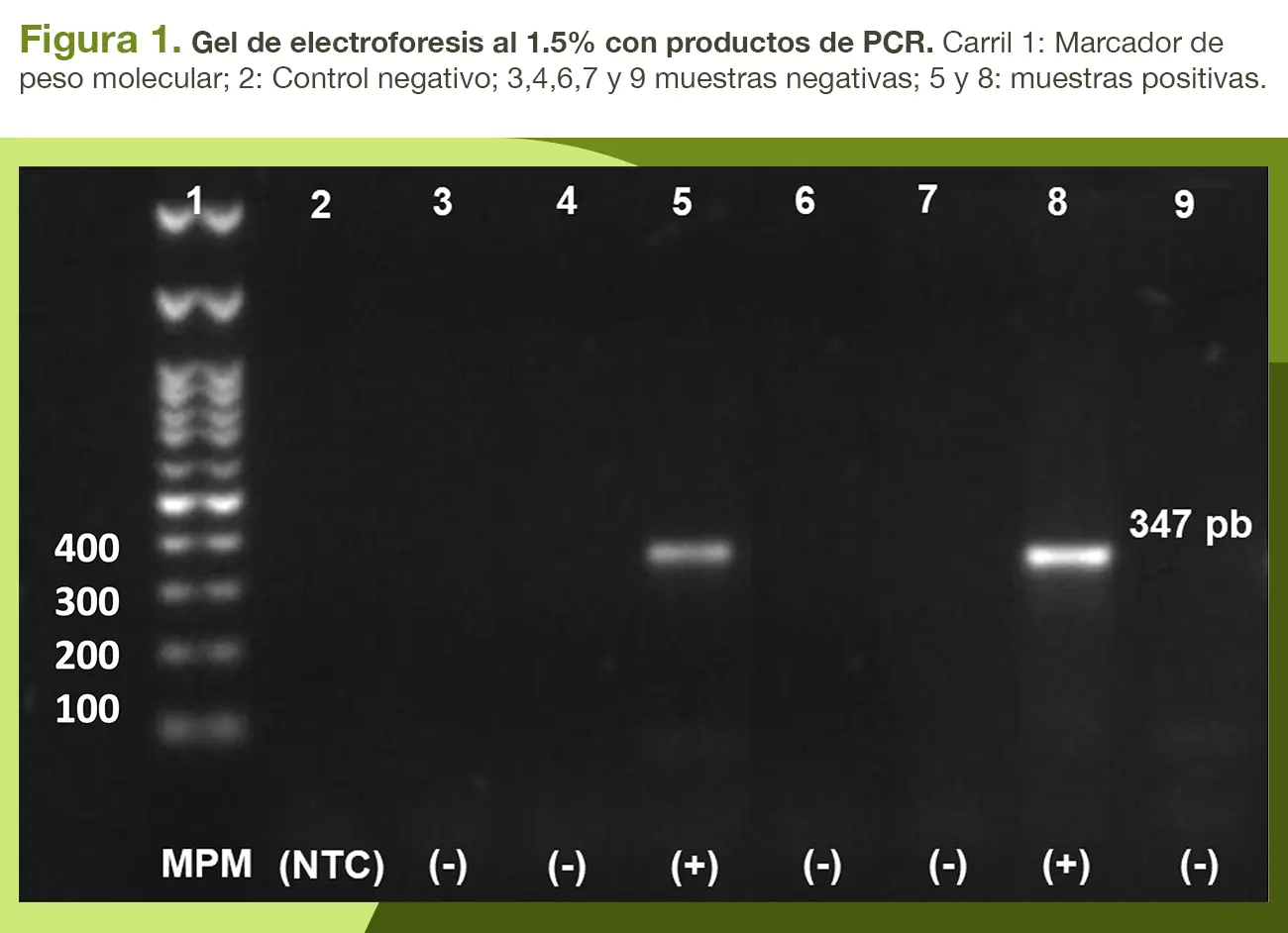
El uso de la PCR con los primers TFR3 y TFR4 para amplificar una región de 347 pb, que incluye el gen 5.8S y las secuencias ITS1 e ITS2 del ADN ribosomal de T. foetus, ha sido ampliamente documentada y validada en varias publicaciones científicas (Madoroba et al 2011; de Oliveira et al 2018; Gharban, 2023). Actualmente la detección molecular de Trichomonas foetus en vacas ha avanzado significativamente en los últimos años, siendo una herramienta crucial para el diagnóstico preciso, ofreciendo como principal ventaja el obtener resultados en pocas horas y sin la necesidad de cultivos caros (Cobo et al., 2007), al igual que en nuestro ensayo en vacas abortadas, con la diferencia que en esos trabajos guiaron sus investigaciones a la prevalencia y no a la estabilidad del protozoario en cultivo alternativo posterior al congelamiento. A pesar de esto, nuestro equipo de trabajo corrobora y recomienda la detección por PCR de T. foetus a partir de piometra, ya que facilita la implementación inmediata de medidas de control y prevención sobre el porcentaje de vacas que quedan infectadas y permanecen es estado de portadoras durante mucho tiempo o permanentemente (Palomares et al., 2017).
Otro factor importante en estudio fue la estabilidad al posterior descongelamiento de las muestras conservadas a 60°C y formular un medio de cultivo alternativo para poder demostrar la viabilidad de T. foetus sin criopreservadores. La motilidad se evaluó en frotis directos obtenidos de la formulación desarrollada y de los medios de cultivo, al observar al microscopio en 100x, al día 4 de las dos muestras de piometra detectadas por PCR. Se observaron pequeños microorganismos con forma ovoide y un pequeño flagelo que se movían de manera espasmódica, característicos de Trichoma foetus (Figura 2). Archelli (2023) describe que, en el campo de observación de las tricomonas, se observan microorganismos con movimientos espasmódicos, con traslación o sin ella, viéndose el flamear la membrana ondulante y los flagelos anteriores. Lo anteriormente descrito coincide con los resultados obtenidos a la observación directa de las siembras positivas, cuyos movimientos eran espasmódicos y ondulantes al día 4.

Con las tinciones de Gemsa se corroboro el desarrollo de T. foetus, notándose una estructura ovoide rosado, con núcleo morado y el característico axostilo. En cuanto al desarrollo de la membrana ondulante y flagelo posterior, solo se alcanzó a observar en pocas trichomonas (Figura 3). Unzaga y Zonta (2023) comentan que las muestras que se incuban a 37ºC y se observan cada 24 horas para detectar el desarrollo del agente, generalmente ocurre entre el día 2 y 4 de incubación. En el presente ensayo, se observó mayor cantidad de trichomonas al día 4, coincidiendo en el rango descrito por el autor.
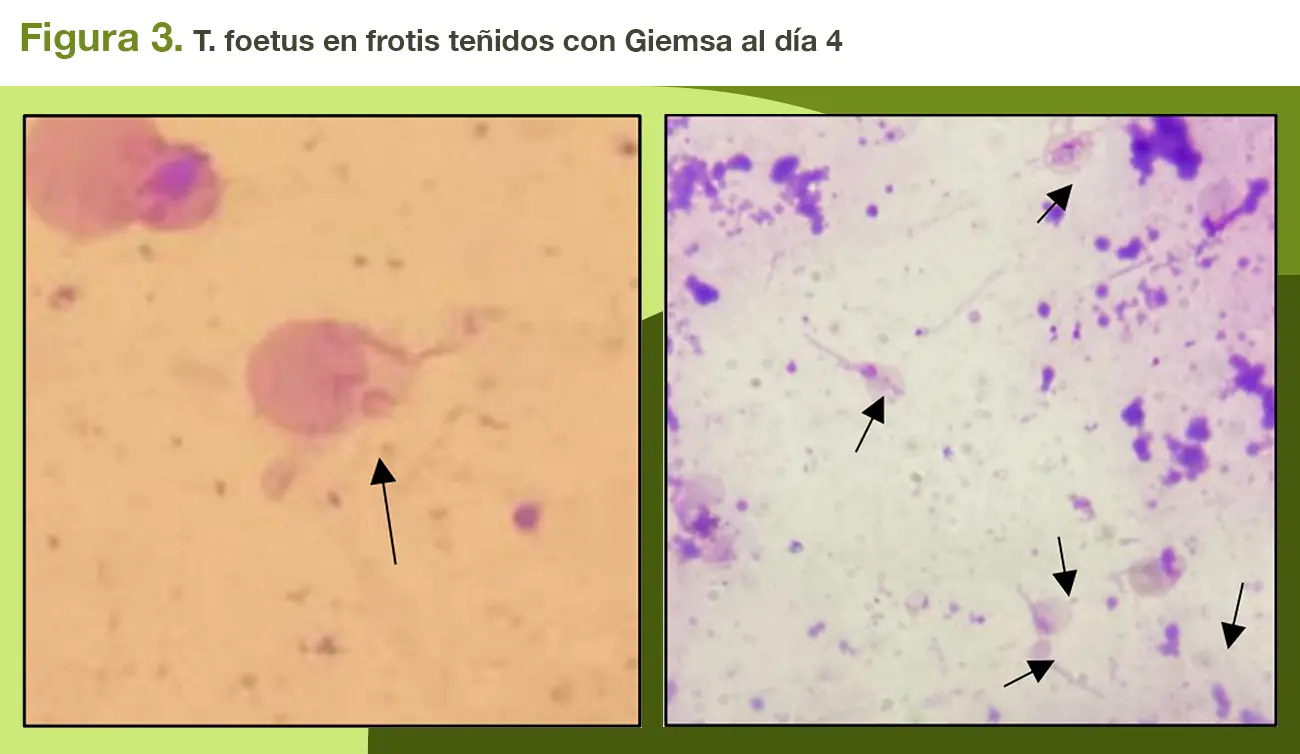
El desarrollo y la motilidad descritas en la microscopia y tinción demuestran la resistencia de Trichomonas foetus a temperaturas bajas, siendo un tema de relevancia en la literatura científica debido a su impacto en la transmisión y persistencia de esta enfermedad parasitaria. Este estudio ha podido confirmar y demostrar que T. foetus puede mantener su viabilidad a temperaturas más bajas de lo esperado sin la necesidad de criopreservadores, lo que puede facilitar su supervivencia en ambientes externos y aumentar el riesgo de transmisión entre animales susceptibles. Esta capacidad de resistencia subraya la importancia de implementar medidas efectivas de control y prevención para limitar la propagación de la enfermedad por inseminación artificial.
Conclusiones
La fórmula del medio de cultivo alterno (TrichonEmma) desarrollado por el equipo trabajo no solo logró que T. foetus mantuviera su integridad para los propósitos de transporte y conservación de la calidad de una muestra como parte integral de un sistema de diagnóstico, sino que también logró que el parasito sobreviviera y se desarrollara posterior al descongelamiento. Esto comprueba que T. foetus puede mantener su viabilidad aún bajo congelamiento sin necesidad de criopreservadores. Por otro lado, el presente estudio es el primer reporte científico en México que identifica molecularmente a T. foetus a partir de piometra de vacas abortadas. Lo anterior comprueba que existen hembras que pueden permanecer como portadoras del protozoario por largos periodos de tiempo, vulnerando la salud del rebaño al contagiar exponencialmente el resto de los animales sanos.
Bibliografía
Archelli, S. M., Radman, N. E., Gamboa, M. I., & Mastrantonio Pedrina, F. L. (2023). Trichomonas vaginalis.
Burgess D.E., McDonald C.M. 1992. Analysis of adhesion and cytotoxicity of Trichomonas foetus to mammalian cells by use of monoclonal antibodies. Infection and immunity 60, 4253-4259.
Cobo, E. R., Campero, C. M., Johnson, S. M., & Corbeil, L. B. (2007). Trichomonas foetus induces apoptosis and secretion of interleukin 8 in bovine vaginal epithelial cells. Infection and Immunity, 75(3), 1687-1692.
Clothier, K. A., Villanueva, M., Torain, A., Hult, C., & Wallace, R. (2015). Effects of bacterial contamination of media on the diagnosis of Tritrichomonas foetus by culture and real-time PCR. Veterinary Parasitology, 208(3-4), 143-149. https://doi.org/10.1016/j.vetpar.2015.01.006.
Cuevas, F. R. (1967). Tricomoniasis en sementales bovinos de la cuenca lechera del Valle de México. Revista Mexicana de Ciencias Pecuarias, (9), 28-a.
de Oliveira Filho, R. B., Malta, K. C., de Melo Borges, J., De Oliveira, P. R. F., dos Santos Filho, G. J., Nascimento, G. G., & Pinheiro Júnior, J. W. (2018). Prevalence and risk factors associated with Tritrichomonas foetus infection in cattle in the state of Paraíba, Brazil. Acta Parasitologica, 63(2). https://doi.org/10.1515/ap-2018-0039. da Silva Silveira, C., Fraga, M., Monesiglio, C., Delpiazzo, R., Macías-Rioseco, M., Giannitti, F., & Riet-Correa, F. (2020). Detection of Tritrichomonas foetus by PCR in preputial smegma of bulls in Uruguay. DOI: 10.29155/VET.56.213.7.
Felleisen, R. S., Lambelet, N., Bachmann, P., Nicolet, J., Müller, N., & Gottstein, B. (1998). Detection of Tritrichomonas foetus by PCR and DNA enzyme immunoassay based on rRNA gene unit sequences. Journal of clinical microbiology, 36(2), 513-519. DOI: https://doi.org/10.1128/jcm.36.2.513-519.1998.
Gharban, H.A.J. (2023). Molecular prevalence and phylogenetic confirmation of bovine trichomoniasis in aborted cows in Iraq. Vet World. 580-587. doi: 10.14202/vetworld.2023.580-587.
Gifford, C., John, W., Jerry, H. (2020). Economic impact of trichomoniasis in New Mexico beef herds. New Mexico State University, College of Agricultural, Consumer, and Environmental Sciences. Guide B-233.
https://aces.nmsu.edu/pubs/_b/B233/welcome.html
Madoroba, E., Gelaw, A., Hlokwe, T., & Mnisi, M. (2011). Prevalence of Campylobacter foetus and Trichomonas foetus among cattle from Southern Africa. African Journal of Biotechnology, 10(50), 10311-10314. 10.5897/AJB11.1259.
Martin, K. A., Henderson, J., & Brewer, M. T. (2021). Bovine trichomonosis cases in the United States 2015–2019. Frontiers in Veterinary Science, 8, 692199. https://doi.org/10.3389/fvets.2021.692199.
Michi, A. N., Favetto, P. H., Kastelic, J., & Cobo, E. R. (2016). A review of sexually transmitted bovine trichomoniasis and campylobacteriosis affecting cattle reproductive health. Theriogenology, 85(5), 781-791.
ttps://doi.org/10.1016/j.theriogenology.2015.10.037
Ondrak, J. D. (2016). Tritrichomonas foetus prevention and control in cattle. Veterinary Clinics: Food Animal Practice, 32(2), 411-423. https://doi.org/10.1016/j.cvfa.2016.01.010.
Palomares, R. A., Hurley, D. J., Crum, L. T., Rollin, E., Collop, T., Williard, A., & Corbeil, L. B. (2017). Serum, uterine, and vaginal mucosal IgG antibody responses against Tritrichomonas foetus after administration of a commercial killed whole T foetus vaccine in beef cows. Theriogenology, 87, 235-241. https://doi.org/10.1016/j.theriogenology.2016.08.031.
Ramírez J.A., Lastra C.C., González E., Grado A., Leyva I., Baxter J. (2017). La Tricomoniasis Bovina y sus Efectos en la Fertilidad. Ponencia. Estudio y proyecto presentado en la EXPOGAN de Chihuahua, Chih. Septiembre, 2017.
Ribeiro, L., Silva, O., Duarte, F., & Jesus, V. (2021). Investigation of Tritrichomonas foetus in cryopreserved bovine semen by culture and polymerase chain reaction. Arquivo Brasileiro de Medicina Veterinária E Zootecnia/Arquivo Brasileiro de Medicina Veterinária E Zootecnia, 73(5), 1023-1028. https://doi.org/10.1590/1678-4162-12370.
Unzaga, J. M., & Zonta, M. L. (2023). Protozoos parásitos de importancia sanitaria: un abordaje transdisciplinar. Libros de Cátedra.
World Organization for Animal Health (WOAH). Chapter 3.4.15, Trichomonosis. OIE TerrestrialManual 2018. https://www.oie.int/fileadmin/Home/eng/Health_standards/tahm/3.04.15_TRICHOMONOSIS.pdf.
Yao, C. (2021). Control and eradication of bovine trichomonosis in Wyoming, USA by testing and culling positive bulls. Veterinary Research, 52(1), 129. https://doi.org/10.1186/s13567-021-00996-w https://doi.org/10.1186/s13567-021-00996-w