Número:
- Vol. 3
- Num. 16
- Julio - Agosto
Porcicultura.com
Autores:
 Mónica
Mónica Zermeño Acosta
Nacionalidad: Mexicana
Grado académico:
 Héctor
Héctor Sumano López
 Jorge
Jorge Luna del Villar
 Lilia
Lilia Gutiérrez Olvera
ISSN-e:
2992-7293
Farmacocinética superior del Hiclato de Doxiciclina en cerdos con una nueva forma farmacéutica administrada en el alimento
Mónica Zermeño-Acosta1, Lilia Gutiérrez-Olvera1*, Jorge Luna-del Villar, Héctor Sumano-López1
1 Departamento de Fisiología y Farmacología, Fac. de Med. Vet y Zoot., UNAM. Ciudad Universitaria 04510, Cd Mx y 2 Departamento de Cirugía, Fac. de Med. Vet y Zoot., UNAM. Ciudad Universitaria 04510 CDMX
Palabras clave: doxiciclina, forma-farmacéutica, biodisponibilidad.
Introducción
Uno de los principales factores de uso de antibacterianos en cerdos son las enfermedades respiratorias, entre las cuales se pueden encontrar una gran diversidad de causas, como bacteris, virus, hongos, etc. El uso de antibacterianos se considera esencial para disminuir la mortalidad cuando se ha diagnosticado que la principal causa es bacteriana, sin embargo con las nuevas normativas que se están imponiendo a nivel mundial para el uso correcto de antibacterianos (Who, 2017), es de gran importancia el diseñar correctamente los fármacos, para que se ajusten a los modelos PK/PD para cada especie, con lo cual se puede aumentar la probabilidad de éxito del tratamiento y disminuir la probabilidad de generación de resistencia antimicrobianas (Vilaró et al., 2020), además del impacto que esto puede tener en bienestar animal y a nivel económico negativo por reducción de la conversión alimenticia, aumento en el número de días para llegar a rastro y por el gasto en medicamentos y decomisos en rastro, (Sumano et al, 2023).
El uso de doxiciclina en el alimento en cerdos, para el tratamiento y control de infecciones respiratorias es una práctica común (Sumano et al., 2023). La doxiciclina es una de las tetraciclina de mayor uso vía oral, en cerdos, por su amplio espectro y excelente penetración tisular, incluyendo sistema respiratorio. Es activa contra un elevado número de microorganismos Gram+, Gram-, micoplasmas, clamidias, ricketsias y algunos protozoos. Se le ha adscrito un punto de inflexión (breakpoint) de 0.25 µg/mL para microorganismos sensibles; 0.5 µg/mL para los medianamente resistentes y 2 µg/mL para los resistentes (Petrocchi-Rilo et al., 2020). A dosis de 11.8 a 13.3 mg/kg/día (calculadas con base en la relación peso: consumo de alimento), administrada en uno o dos pulsos, las concentraciones de doxiciclina séricas logradas en el estado estable (ss) oscilan entre 0.7 y 1.0 µg/mL. En comparación con otras especies la biotransformación de doxiciclina en cerdos es muy baja y se concluye que tiene una T½β (vida media de eliminación) más corta que la reportada en otras especies, 4 h después de la aplicación IV de 10 mg/kg (Riond y Riviere, 1990), no se utiliza por vía intramuscular debido a la necrosis que induce en el sitio de administración. A pesar de todo esto, la administración oral de doxiciclina se hace sin ningún diseño farmacéutico. Apelando a la sugerencia de que se deben desarrollar formulaciones apropiadas y no solamente agregar el principio activo al alimento como un polvo (Riond y Riviere, 1990), se estableció como hipótesis de trabajo y objetivo de este ensayo realizar un diseño de doxiciclina exprofeso para cerdos y que resultase en variables farmacocinéticas superiores. Finalmente, una doxiciclina optimizada será más útil para las empresas porcícolas y con ello se le puede dar mayor viabilidad al principio activo como elemento terapéutico. Con este fin se utilizó un sistema de patente UNAM (MX/a/2012/013222) denominados como FOLA (F=biodisponibilidad, O=optima, LA=larga acción), los cuales contienen vehículos que mejoran la biodisponibilidad de los preparados, además de ajustar el proceso de absorción dependiendo del pH de los sitios donde debe absorberse el principio activo.
Objetivo
Evaluar un nuevo preparado farmacéutico de clorhidrato de doxiciclina en pellet para mezclar en el alimento en cerdos, que mejoré la biodisponibilidad (F) y proporcioné un mayor tiempo medio de residencia (MRT), con este fin se va a administrar tipo bolo y ad libitum a una dosis de 20 mg/kg de peso corporal y se va a comparar con el producto original de uso en cerdos.
Material y métodos
Se utilizaron 32 cerdos de 30 días de edad, clínicamente sanos, sin medicación previa al momento del estudio, con un peso promedio de 10 kg ± 1,6 kg, de las áreas de destete dos y tres. Los animales se separaron aleatoriamente en grupos de 8 cerdos cada uno, y para cada corrida se realizó una lista determinando la dosis de fármaco correspondiente al peso de cada cerdo. Se asignó un corral a cada grupo y cada cerdo se identificó numéricamente en el lomo con un marcador de ganado, asignándose un color diferente a cada grupo. El alimento y el agua se administraron ad libitum según el manejo del rancho. Se confirmó que el alimento no contenía ningún tipo de antibacteriano, y que los cerdos elegidos no tengan algún tratamiento antibacteriano previo. Para los grupos de dosis tipo bolo cada animal se dosificó individualmente con dosis tipo bolo. En cada caso se contó con un grupo control, el cual correspondió al antibacteriano administrado en alimento o agua, según sea la presentación del producto original (de patente) para uso en cerdos. Posterior a la dosis en bolo forzado, se tomaron muestras de sangre mediante punción yugular con Vacutainer sin anticoagulante en tiempos predeterminados y con asistencia técnica en los siguientes intervalos: hora cero (antes de la medicación) y post administración: 30 min, 1, 2, 4, 6, 8, 10, 12 y 24 h. Cada muestra se identificó con el grupo, el número de cerdos y el tiempo de muestreo, ningún cerdo fue muestreado más de 5 veces. Inmediatamente la sangre se centrifugó a 3500 rpm durante no más de 10 min para obtener el suero, el cual se recogió con pipetas Pasteur y se depositó en tubos de criopreservación, identificados con la misma leyenda que el tubo de origen, y se congeló a - 20 ºC hasta el análisis. El análisis de doxicyclina se realizó mediante la técnica establecida por Axisa et al. (2000). Se construyó una curva estándar para la doxiciclina utilizando muestras de suero combinadas sin antibióticos recolectadas de cerdos sacrificados y no medicados. El coeficiente de varianza intraensayo fue <2,0 y el error entre ensayos fue <2,2. El ensayo analítico fue lineal en un rango de concentraciones de 0,1 a 50 µg/ml. La recuperación media ± 1 DE fue de 94 ± 1,8% (r = 0,96). El límite de detección fue de 0,07 µg/mL y el límite de cuantificación fue de 0,1 µg/mL.
Para los estudios farmacocinéticos se utilizó el programa PKAnalyst, donde la dosis bolo se ajustó al modelo 3, de dos compartimentos con entrada de primer orden y salida de primer orden (r ≥ 0,99) y la dosificación ad libitum se ajustó al modelo 13 de dos compartimentos con entrada de primer orden y salida de primer orden (r ≥ 0,99). Los parámetros farmacocinéticos determinados fueron: K½ab = constante de semivida de absorción; CMAX = concentración plasmática máxima alcanzada; TMAX = tiempo para alcanzar Cmax; AUC = área bajo la curva de concentración plasmática de doxiciclina a lo largo del tiempo; AUMC = área bajo la curva de concentración sérica de doxiciclina tiempo/tiempo; MRT = tiempo medio de residencia; AUCT = área bajo la curva de la concentración plasmática de doxiciclina a lo largo del tiempo por el método trapezoidal. Los datos se presentan como media ± 1DE de 8 observaciones para cada parámetro y comparaciones estadísticas de Cmax, Tmax, AUC, MRT y T½β entre los grupos. El análisis estadístico incluyó las pruebas de Kruskal-Wallis y Dunn.
Resultados y discusión
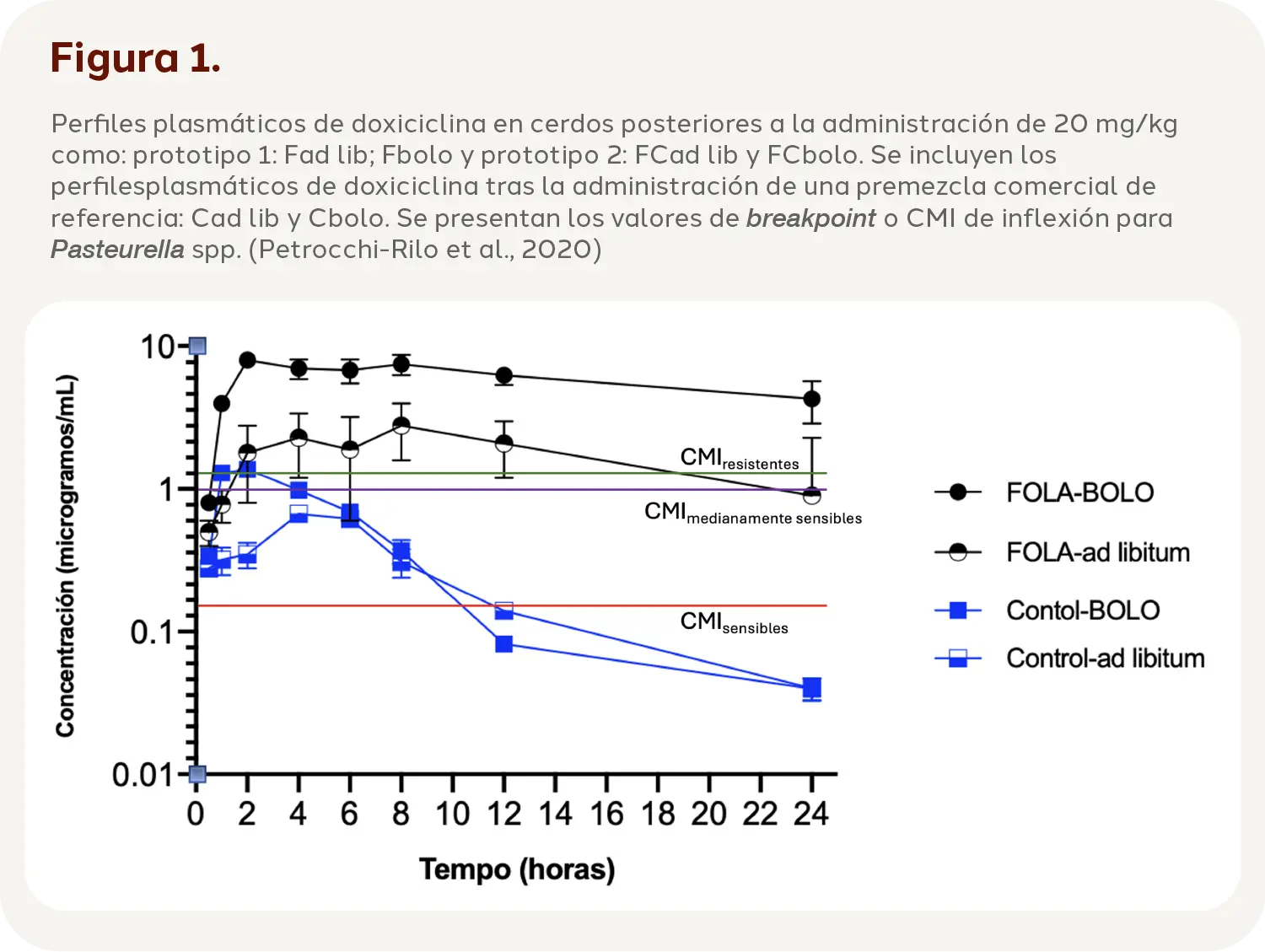
En el cuadro 1 y la figura 1 se resumen los datos logrados con los dos prototipos (Fad-lib y Fbolo y FCad-lib y FCbolo) y los obtenidos para el grupo control o de referencia (Cbolo y C adlib). En el cuadro se resaltan las diferencias estadísticamente significativas, que incluyen mayores valores de F (P < 0.05) y de RT
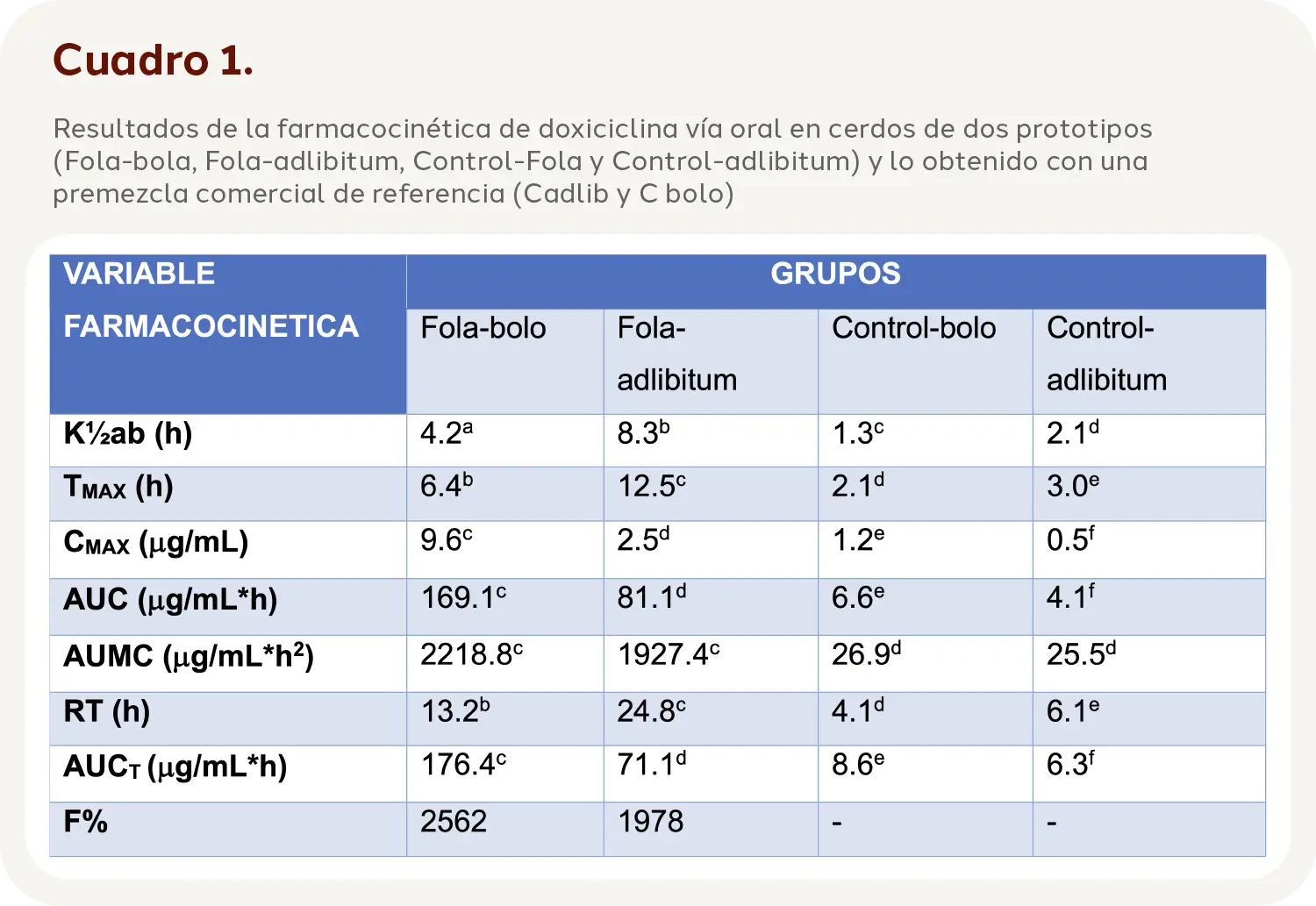
K½ab = constante de vida media de absorción; CMAX = concentración plasmática máxima lograda; TMAX = tiempo para lograr Cmax; AUC= área bajo la curva de concentración plasmática de doxiciclina en el tiempo; AUMC = área bajo la curva de concentración plasmática de doxiciclina en el tiempo/tiempo; RT = Tiempo medio de residencia; AUCT = área bajo la curva de concentración plasmática de doxiciclina en el tiempo por el método trapezoidal. F= biodisponibilidad calculada vs su control
a, b, c Diferentes literales significan diferencias estadísticas entre columnas (P< 0.05).
Conclusiones
Los resultados de la presente investigación indican que es factible mejorar las variables farmacocinéticas de la doxiciclina en cerdos, lograr concentraciones notablemente elevadas de doxiciclina en el plasma de cerdos y por lo tanto en tejidos utilizando los prototipos del principio activo diseñados exprofeso. Si se considera que la doxiciclina es un antibacteriano tiempo dependiente, que requiere estar al menos el 60% del intervalo de dosificación al menos 2-4 veces la CMI, las concentraciones que se logran son incluso superiores al denominado breakpoint de bacterias resistentes (2 µg/mL) (Petrocchi-Rilo et al., 2020) y dado un valor elevado de tiempo medio de residencia (RT) por un tiempo mucho mayor que la doxiciclina de referencia o premezcla estándar sin diseño farmacéutico. La F comparativa o Fr (bioequivalencia relativa) del mejor prototipo ad libitum (FOLA-adlibitum) contra el referente administrado ad-libitum (Contol-adlibitum) fue mayor a 2000%, lo que indudablemente marcará una notable diferencia clínica. Particularmente en casos desafiantes de patógenos con algún grado de resistencia. Es importante destacar que ni los prototipos probados ni el alimento medicado de referencia indujeron ningún cambio en el consumo de alimento ni en la deposición y consistencia de las heces de los cerdos. La forma de administración no implicó modificaciones en los patrones de consumo de alimento medicado ni reacciones visibles de alteración de los patrones digestivos. Además, queda por realizar ensayos a escala industrial para verificar los datos de compatibilidad con varias dietas y la aceptación por diferentes edades y grupos de cerdos. Asimismo, será fundamental realizar modelos PK/PD para optimizar las dosis de este antibiótico y analizar si las concentraciones alcanzadas impactan en las curas bacteriológicas en brotes de enfermedades bacterianas. Finalmente, de acuerdo con los estándares propuestos por la Agencia Europea de Medicamentos para la liberación modificada de preparaciones farmacéuticas, el valor obtenido para los prototipos fabricados (ARAUC < 1,55) podría considerarse como que conduce a una acumulación no relevante del fármaco (Scheerans et al., 2015). Se necesitan más investigaciones para asegurar el tiempo residual de estas nuevas formulaciones de doxiciclina. Resta realizar ensayos a escala industrial para verificar los datos y analizar si las concentraciones logradas repercuten en curas bacteriológicas amén de clínicas en campo.
Fuente financiadora
Proyectos PAPIIT-UNAM: IT200222
Referencias bibliográficas
Petrocchi-Rilo M, Gutiérrez-Martín CB, Pérez-Fernández E, Vilaró A, Fraile L, Martínez-Martínez S. (2020). Antimicrobial Resistance Genes in Porcine Pasteurella multocida Are Not Associated with Its Antimicrobial Susceptibility Pattern. Antibiotics (Basel). 9(9): 17. doi: 10.3390/antibiotics9090614
Riond, J.L, Riviere, J.E. (1990) Pharmacokinetics and metabolic inertness of doxycycline in young pigs. Am J Vet Res. Aug;51(8):1271-5.
Sumano L, H, Ocampo C, L, Gutiérrez O, L. (2023). Farmacología Veterinaria 1ª edición Universidad Nacional Autónoma de México. ISBN 978-607-30-8146-7
Vilaró A, Novell E, Enrique-Trancon V, Balielles J, Allué E, Fraile L. (2020). Antimicrobial stewardship for respiratory psthogens in swine. ANTIBIOTICS (Basel). 9(11):727. doi:10.3390/antibiotics9110727
WHO 2017. Guidelines on use of medically important antimicrobials in food-producing animals.
chrome-extension://efaidnbmnnnibpcajpcglclefindmkaj/https://iris.who.int/bitstream/handle/10665/258970/9789241550130-eng.pdf?sequence=1